Обращение - ряд
Cтраница 1
Обращение ряда, в котором элементы расположены в соответствии с их способностью к комплексообразованию, приводит к обращению экстракционного ряда. Здесь наблюдается та же закономерность, которая, по-видимому, имеет место при экстракции лантаноидов из разбавленных растворов HNO3 при помощи ТБФ. [1]
Обращение ряда спиртов по относительной кислотности между газовой фазой и протонными растворителями ( трет - ЕиОН EtOH МеОН) приписано также стерическим затруднениям для сольватации [107] ( см., однако, стр. [2]
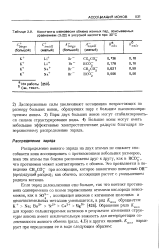 |
Константы оавновесия обмена ионных пар, описываемых уравнением в уксусной кислоте при 30 С. [3] |
Обращение ряда Kass для хорошо сольватируемых катионов в результате изменения структуры аниона имеет исключительную важность для интерпретации селективности ионного обмена ( разд. [4]
Обращение ряда анионов в R N X - представляет собой явление, аналогичное описанному впервые Эвансом ( разд. [5]
Обращение ряда избирательности анионов может иметь место и в разделениях на органических ионитах, если вводить в состав элюентов апротонные растворители, в которых анионы подвергаются лишь ион-дипольной сольватации без образования водородных связей. Как следствие, крупные и легко деформирующиеся анионы сольватируются сильнее и легче десорбируются с анио-нита. Например, с колонки с анионитом Дауэкс - 1Х4 в N0 - форме 0 1 N NaNOg в диметилформамиде ( ДМФА) легко десор-бирует анионы SCN, не затрагивая остальные анионы. [6]
Обращение ряда классов матриц может быть достигнуто значительно более экономичными, чем в общем случае, методами. [7]
Обращение ряда термической устойчивости наблюдается и в тех случаях, когда внешнесферный анион характеризуется тенденцией к образованию ковалентных связей с данным центральным ионом. [8]
Обращению ряда содействует также уменьшение энергии решетки комплексной соли от хлорида к иодиду. Радиусы аквокатионов меньше, чем радиусы амминокатионов, в связи с чем убывание U становится более заметным. По этой причине уже в случае гидратов марганца ( II) и кобальта ( II) наблюдается явление обращения, в то время как для аммиакатов солей этих же металлов - наблюдаются нормальные ряды термической устойчивости. [9]
Задачу обращения рядов Арбогаст сводит к рассмотренной выше задаче преобразования рядов. [10]
Подобного рода обращение ряда кинетической и термодинамической устойчивости следует отнести к разнице скоростей образования обоих комплексов в выбранных условиях. Данные табл. 2 соответствуют этому выводу. [11]
С задачей обращения ряда мы сталкиваемся каждый раз, когда необходимо определить функцию, обратную к данной функции, если последняя задана в виде степенного ряда. [12]
Заметим, что мультиплетная теория объясняет обращение рядов, указанное выше, тогда как другие теории катализа не дают для него объяснения. [13]
Кроме того, опыт не подтверждает обращения ряда d dl - d2 при замене л-донорных молигандов на л-акцепторные. По-видимому, уменьшение трансвлияния при переходе от d к dz определяется не столько усилением шгс-отталкивапия, сколько общим перераспределением электронной плотности по МО ( изменением коэффициентов при АО в МО) при понижении степени окисления металла. [14]
Авторы считают, что ответственным за обращение ряда устойчивости для галогенидных комплексов в указанных трех растворителях являются изменения энтальпии при образовании Т1Х; на это в свою очередь сильно влияют изменения при сольватации галогенид-иона. Из приведенных примеров следует, что при изучении влияния сольватации на комплексообразование нельзя пренебрегать взаимодействиями между лигандом и растворителем. [15]
Страницы: 1 2 3 4