Обрыв - радикал
Cтраница 1
Обрыв растущих макромолекулярных радикалов происходит в результате бимолекулярной реакции между ними. [1]
Возможен и другой случай - когда скорость обрыва радикалов на поверхности катализатора больше скорости их зарождения. [2]
Уменьшение константы обрыва объясняется [23] тем, что обрыв радикалов контролируется диффузией, которая, в свою очередь, уменьшается с давлением из-за роста вязкости среды. Сейчас эта точка зрения считается достаточно обоснованной и ускорение полимеризации с давлением часто связывается не только с увеличением константы роста, но и с падением скорости обрыва из-за повышения вязкости среды. [3]
Общая теория гомогенно-гетерогенных реакций в потоке применена к радикально-цепным реакциям с зарождением и обрывом радикалов на стенке. Получены выражения для соотношений выходов различных продуктов и указаны критерии для случая, когда основную роль играет зарождение ( обрыв) радикалов на стенке по сравнению с зарождением ( обрывом) в объеме. [4]
Величина тангенса угла наклона прямой ( рис. 3), равная 0 482, свидетельствует о бирадикальном механизме обрыва радикалов ROa - Высказано предположение о характере механизма образования карбонильных и гидроксильных групп. [5]
Такой механизм изолирования радикалов, являющийся специфическим для эмульсионной полимеризации, позволяет значительно повысить концентрацию растущих радикалов по сравнению с другими процессами при равных скоростях инициирования вследствие невозможности взаимного обрыва радикалов из разных латексных частиц. Это позволяет получать полимеры с высокими молекулярными массами при скоростях реакции, значительно превышающих скорости полимеризации в блоке и растворе. Достоинством данного способа является также легкость теплоотвода. [6]
 |
Зависимость периода индукции окисления полипропилена от состава смеси 2 4 6-три-трет. бутидфенола и ДЛТДП при температуре 200 i - - кислорода 200 мм рт. ст. [7] |
Поэтому смеси стабилизаторов ингибирующих свободно-радикальные процессы с фосфитами должны обнаруживать синергичеекий эффект, механизм которого, так же, как и в присутствии других разрушителей гидроперекиси, будет состоит из обрыва радикалов и подавления разветвления цепей. [8]
В дисперсионной полимеризации размер образующихся частиц полимера, их относительно низкая способность к абсорбции мономера и, соответственно, высокая внутренняя вязкость, а также высокие скорости инициирования - способствуют затруднению обрыва радикалов в частицах и создают условия для сосуществования многих радикалов в каждой частице в течение всего процесса полимеризации. Увеличение скорости, наблюдаемое в дисперсионной полимеризации, возникает из-за затруднения процесса обрыва радикалов в частицах полимера, точно так же как и при полимеризации в массе; поэтому процесс можно рассматривать как микроблочную полимеризацию. В этом случае возможен обмен радикалов между частицами, вследствие легкости выхода из частицы малых подвижных радикалов, образуемых в реакциях передачи цепи на этот мономер. [9]
Следовательно, удвоение скорости инициирования не приводит к увеличению скорости полимеризации в два раза; она возрастает только в У 2 раза. Такое поведение объясняется бимолекулярным механизмом обрыва радикалов. [10]
Действие поверхности сводится к инициированию или обрыву радикалов или ионов, которые диффундируют в гомогенную фазу, газ или жидкость, где протекает цепная реакция. Если инициирование на поверхности проходит очень быстро, то вероятно, что и обрыв эффективен на поверхности. Если активные центры не заменяются в реакции, то такой вывод вытекает из принципа детального равновесия. Такие системы могут быть выявлены на основании того факта, что удельные скорости в них почти не зависят от отношения поверхность / объем, т.е. имеют нулевой порядок по поверхности или катализатору. [11]
Действие поверхности сводится к инициированию или обрыву радикалов или ионов, которые диффундируют в гомогенную фазу, газ или жидкость, где протекает цепная реакция. Если инициирование на поверхности проходит очень быстро, то вероятно, что и обрыв эффективен на поверхности. Если активные центры не заменяются в реакции, то такой вывод вытекает из принципа детального равновесия. Такие системы могут быть выявлены на основании того факта, что удельные скорости в них почти не зависят от отношения поверхность / объем, т.е. имеют нулевой порядок по поверхности или катализатору. [12]
В дисперсионной полимеризации размер образующихся частиц полимера, их относительно низкая способность к абсорбции мономера и, соответственно, высокая внутренняя вязкость, а также высокие скорости инициирования - способствуют затруднению обрыва радикалов в частицах и создают условия для сосуществования многих радикалов в каждой частице в течение всего процесса полимеризации. Увеличение скорости, наблюдаемое в дисперсионной полимеризации, возникает из-за затруднения процесса обрыва радикалов в частицах полимера, точно так же как и при полимеризации в массе; поэтому процесс можно рассматривать как микроблочную полимеризацию. В этом случае возможен обмен радикалов между частицами, вследствие легкости выхода из частицы малых подвижных радикалов, образуемых в реакциях передачи цепи на этот мономер. [13]
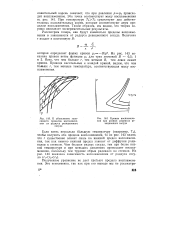 |
К объяснению зависимости пределов воспламенения от радиуса реакционного сосуда.| Кривые воспламенения при разных радиусах реакционного сосуда. [14] |
Если взять несколько большую температуру ( например, Т4), чтобы получить оба предела воспламенения, то из рис. 143 видно, что г существенно влияет лишь на нижний предел воспламенения, так как именно нижний предел зависит от диффузии радикалов к стенкам. Чем больше радиус сосуда, тем при более низкой температуре и при меньших давлениях происходит воспламенение, поскольку тем труднее обрыв радикала на стенках. [15]
Страницы: 1 2