Обрыв - цепь - окисление
Cтраница 1
Обрыв цепи окисления может произойти в результате рекомбинации радикалов с образованием стабильных в данных условиях соединений. [1]
Обрыв цепей окисления в растворах этих соединений протекает по аналогичному механизму с участием перекисных радикалов. [2]
Следовательно, многократный обрыв цепей окисления осуществляется только в присутствии металлокомплексов, в которых для центрального атома характерны одноэлектронные переходы. [3]
Вопрос о возможности обрыва цепи окисления в процессе термоокислительной деструкции полимера за счет связывания фосфитами свободных RO - и ROO - радикалов ( I - 1 2) является дискуссионным. [4]
Участие фенола в иных реакциях, чем радикальный обрыв цепи окисления или разрушение гидроперекисей, ак правило; снижает эффекти-внбсть антиоксиданта. Так, имеется указание ( 2), что образование водородных связей между фенолом и кислородсодержащими группами, накапливающимися в углеводороде, при окислении снижает их эффективность в основной реакции обрыва цепи. Поэтому исследование реакционной способности фенолов в реакции образования водородной связи представляет само по себе значительный теоретический интерес. [5]
Выполнение неравенств является необходимым условием для осуществления многократного обрыва цепей окисления на соединениях переходных металлов. [6]
Весьма заманчивым представляется изучение таких случаев, где наблюдается многократный обрыв цепей окисления на молекуле ингибитора. [7]
Вероятно, синергизм действия смеси амина и сульфида объясняется тем, что первый компонент при обрыве цепи окисления дает молекулу гидроперекиси ( см. выше), а второй разрушает ее, увеличивая время жизни первого компонента ( амина), поскольку уменьшается число окислительных цепей. Амины и фенолы более эффективны при низких температурах окисления, а превентивные антиоксиданты - при высоких. [8]
Вероятно, синергизм действия смеси амина и сульфида объясняется тем, что первый компонент при обрыве цепи окисления образует гидропероксидную группу ( см. выше), а второй разрушает ее, увеличивая время жизни первого компонента ( амина), поскольку уменьшается число окислительных цепей. Амины и фенолы более эффективны при низких температурах окисления, а превентивные антиоксиданты - при высоких. [9]
Комплекс NiLz является удобньш объектом для исследования, поскольку для соединений М ( П) механизм одноэлектронного обрыва цепей окисления с участием d - - электронов маловероятен и, следовательно, антиокислительные свойства Ш Lz можно отнести к его координированным WH-группам. [10]
Если Со111 при этом не восстанавливается быстро с образованием радикалов, то такая реакция приводит к обрыву цепей окисления. [11]
Таким образом, координация соединениями переходных металлов функциональных групп органических ингибиторов позволяет повысить их эффективность в обрыве цепей окисления, а также при разложении гидроперекисей. [12]
Большое влияние на скорость окисления оказывают антиокислители ( ингибиторы) - вещества, добавление которых приводит к обрыву цепей окисления. Среди них наибольшее значение имеют окислители фенольной природы ( стр. [13]
Если Со 1 при этом не восстанавливается быстро с образованием радикалов, то такая реакция приводит к обрыву цепей окисления. [14]
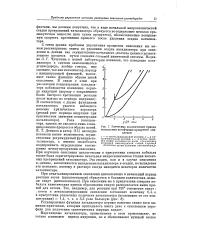 |
Расчетные кинетические кривые накопления устойчивых продуктов окисления. [15] |
Страницы: 1 2