Анализ - элюат
Cтраница 2
Количественный анализ производится в результате обменной реакции на колонках, заполненных соответствующим адсорбентом, и состоит из следующих операций: подготовки ионита для заполнения колонки, подготовки колонки, фильтрации анализируемого раствора через слой ионита, анализа элюата или фильтрата, регенерации ионита. [16]
Одним из наиболее значительных преимуществ этого метода является его пригодность для исследования очень небольших количеств белка или пептидов. Это особенно ценно, например, для анализа разбавленных элюатов, получаемых при хроматографии и гель-фильтрации. Диск-электрофорез позволяет анализировать эти элюаты без предварительного концентрирования. [17]
Хотя объем кварцевой проточной кюветы составляет всего 10 1 - 10 - 2 мл, при прохождении вещества через кювету и соединительные шланги происходит заметное уширение пиков. Тем не менее проточные УФ-денситометры стали незаменимым инструментом анализа элюатов в колоночной хроматографии белков, в частности при фракционировании с помощью ГПХ в циркуляционном режиме и при работе на микроколонках. [18]
ДНФ-аминокислоты фракционируют в аммонийноацетатном буферном растворе ( рН 4 - 10) с ионной силой 0 2 иногда с добавлением этанола. Скорость элюирования 1 мл за 8 мин при 22 С; анализ элюата проводят путем определения оптической плотности. [19]
Данные по сорбции ионов меди, цинка и железа, определенные на основании результатов анализа элюатов, приведены в таблице. [20]
В принципе возможны три методики: а) проявление пятен in situ непосредственно на бумаге, б) проявление после перенесения отпечатка или после диффузии содержимого пятна и пористую среду или гель, в) анализ элюата. [21]
Хроматографию проводят на термостатированной колонке ( 2 5X ХЮО см) с биогелем А-15 ( 100 - 200 меш) ( Bio-Rad. В качестве образца наносят 0 4 - 0 8 мл рибосомального препарата с поглощением примерно 3 00 при 260 нм. Анализ элюата ведут, измеряя оптическую плотность при 260 нм. [22]
 |
Концентрационная трубка для определения про. [23] |
Через трубку порциями по 0 2 - 0 3 мл пропускают диметилформамид. Собирают 2 мл элюата в бюксы или пробирки с пришлифованными пробками. Анализ элюата после перемешивания проводят не позже чем через 5 мин. [24]
Кончик пипетки, которой вносят элюент, должен быть изогнут вверх, чтобы не взмучивать верхний слой носителя. Анализ элюата осуществляют турбидиметрически. [25]
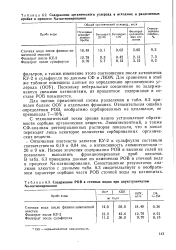 |
Содержание органического углерода в исходных и разделенных пробах в процессе Na-катионирования.| Содержание РОВ в сточных водах при двухступенчатом Na-катионировании. [26] |
В табл. 6.3 приведены данные по изменению РОВ в сточной воде в процессе Na-катионирования. Сопоставление результатов анализов элюатов с данными табл. 6.3 свидетельствует о необратимом характере сорбции части РОВ сточной воды на катионитах. [27]
Наиболее эффективным методом исследования РТФ является хроматографическое разделение олигомеров по типам функциональности с последующим измерением Мп и Ма отдельных фракций и расчетом fn и fw и функций РТФ. При этом выбор того или иного варианта хроматографического метода зависит от класса исследуемых олигомеров. В настоящее время для разделения олигомеров используют колоночную адсорбционную хроматографию, тонкослойную хроматографию и гель-проникающую хроматографию. Колоночая адсорбционная хроматография может проводиться в различных режимах элюирования, отличаться способами загрузки образца, подготовки асадки - силикагеля, анализа элюата и масштабностью фракционирования. Впервые колоночная хроматография на силикагеле с использованием диоксана в качестве элюента была применена для исследования молекулярио-массового распределения олигомеров. [28]
По окончании опыта излишнюю жидкость отсасывают с концов блока и разрезают его на секции. Каждую часть блока элюируют буферным раствором на небольшом фильтре из пористого стекла или во избежание разбавления каждую секцию центрифугируют и промывают на центрифуге. Недостатком этого метода является неполное извлечение образца. Белки с низким молекулярным весом проникают внутрь зерен крахмала и не могут свободно двигаться. Из зерен крахмала вымываются различные вещества, например углеводы, и при анализе элюатов это следует учитывать. [29]
Для аналитических целей до сих пор применяют цитратные буферы, дающие вполне удовлетворительное разделение следов редкоземельных металлов. Поэтому при выборе условий проведения анализа следует принимать компромиссное решение. Сначала элюируются элементы с большим атомным номером, образующие с лимонной кислотой более устойчивые комплексы. Этот метод очень удобен для разделения радиоактивных изотопов и широко применяется при анализе продуктов ядерного расщепления. Для облегчения анализа элюата применяли нейтронную активацию природных редких земель [6, 41 ]; однако при разделении больших количеств веществ чаще используют спектрофотометрические [30, 84] и спектрографические [18, 89] методы ( ср. [30]
Страницы: 1 2 3