Кажущийся мольный объем
Cтраница 1
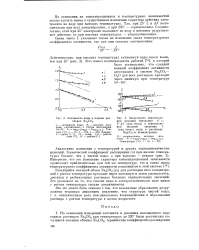 |
Зависимость относительной мольной энтальпии А T-& S ( кал. / моль ц относительной мольной энтропии Л ( кал. / моль воды в растворах Na2C03 от концентрации. [1] |
Кажущийся мольный объем Na2C03 ( pv) для растворов всех концентраций с ростом температуры проходит через максимум и затем уменьшается, достигая в разбавленных растворах больших отрицательных значений. Это указывает на то, что сжатие воды в электростатическом поле ионов с ростом температуры сильно увеличивается. [2]
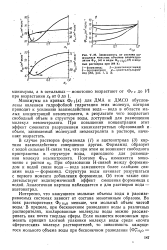 |
Зависимость от состава кажущихся мольных объемов неэлектролитов Фу2 ( а и воды Фу pj2o ( в водных растворах при 298 К. [3] |
Интересно, что кажущиеся мольные объемы воды в рассматриваемых системах зависят от состава монотонным образом. [4]
Так как в расчетах зарядов ионов использованы данные кажущихся мольных объемов при бесконечном разведении, то полученные данные относительно зарядов применимы лишь к разбавленным растворам. [5]
Парциальный мольный объем близок по физическому смыслу к кажущемуся мольному объему и, определяемому следующим образом. Пусть по-прежнему раствор содержит лх моль растворителя и л2 моль растворенного вещества. [6]
Парциальный мольный объем близок по физическому смыслу к кажущемуся мольному объему v, определяемому следующим образом. Пусть по-прежнему раствор содержит пг моль растворителя и 2 моль растворенного вещества. [7]
Парциальный мольный объем близок по физическому смыслу к кажущемуся мольному объему у, определяемому следующим образом. Пусть по-прежнему раствор содержит п моль растворителя и па моль растворенного вещества. [8]
Для характеристики поведения электролита при его растворении пользуются понятием кажущегося мольного объема ( ру), принимая условно, что объем растворителя ( воды) при растворении не изменяется. [9]
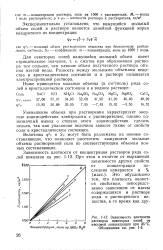 |
Зависимость плотности. [10] |
Величины ф0 и Sv могут быть разложены на ионные составляющие, что позволяет рассчитать кажущиеся мольные объемы растворенной соли по соответствующим объемам ионных составляющих. [11]
 |
Изменение парциального мольного объема этанола в смесях с водой с концентрацией при различных температурах. [12] |
Другой подход к изучению тонких особенностей зависимости объемных эффектов от состава основан на исследовании кажущихся мольных объемов. [13]
С помощью различных экспериментальных методов, таких как измерение давления пара [254-256] и теплоты смешивания [256- 261], ИК-спектроскошш [262-264] и определение кажущегося мольного объема [261, 265, 266], был установлен факт взаимодействия нейтральных фосфорорганических эфиров с различными органическими разбавителями. Предположение о таком взаимодействии было сделано ранее на основе данных по распределению. [14]
Здесь у 1 совпадает с у в уравнении (1.57), h - число гидратации ( в молях воды на 1 моль соли), г - отношение кажущихся мольных объемов соли и растворителя. [15]
Страницы: 1 2