Кажущийся мольный объем
Cтраница 2
Эта закономерность аналогична полученной для водных растворов. Позже Ганн и Грин 5Э определили кажущийся мольный объем нескольких электролитов в жидком, аммиаке при 0 С и обнаружили, что формы кривых, выражающих зависимость кажущегося мольного объема V от с, весьма схожи для галогенидов некоторых щелочных металлов, галогенидов аммония и нитрата бария. Правило аддитивности ионов соблюдается даже при концентрациях, при которых можно было бы ожидать образования значительного количества ионных пар. [16]
Используя вышеупомянутые уравнения, мы рассчитываем заряд ионов титана и гафния. В качестве парциальных мольных объемов использованы данные кажущихся мольных объемов ионов, экстраполированные на бесконечное разведение и равные для Ti, Ш4 иТЮ2 - 13.7, - 3.8 и 14.2 мл / г-ион соответственно. Как известно, титан и гафний в растворах могут находиться в катионной и анионной формах. Если предположить, что элементы присутствуют в анионной форме, то, по уравнению ( 2), величины заряда ионов гафния и титанил-сульфата имеют отрицательное значение. Последнее недопустимо, так как в уравнении ( 2) используется абсолютная величина заряда. Следовательно, для расчета зарядов ионов гафния и тита-нилсульфата применимо лишь уравнение ( 1), предложенное для катионов. [17]
 |
Положение и относительная глубина минимумов VJ некоторых одноатомных и двухатомных спиртов. [18] |
К сожалению, в литературе имеется мало надежных данных о предельных величинах dVJ / dx при X2 - Q. Однако о близкой по смыслу величине предельного наклона кажущегося мольного объема в литературе имеется достаточно данных. [19]
Эта закономерность аналогична полученной для водных растворов. Позже Ганн и Грин 5Э определили кажущийся мольный объем нескольких электролитов в жидком, аммиаке при 0 С и обнаружили, что формы кривых, выражающих зависимость кажущегося мольного объема V от с, весьма схожи для галогенидов некоторых щелочных металлов, галогенидов аммония и нитрата бария. Правило аддитивности ионов соблюдается даже при концентрациях, при которых можно было бы ожидать образования значительного количества ионных пар. [20]
 |
Кажущиеся мольные объемы ( в с. адЗ и числа сольватации катионов в сернокислых растворах их кислых сульфатов. [21] |
Плотности растворов 71 110 большинства веществ были измерены при 25 С. Растворы NaHS04 и KHSO4 были изучены также при 10 и 40 С. По величине кажущегося мольного объема электролита F, который может быть вычислен из плотности раствора, можно получить дополнительную информацию о взаимодействии между ионами электролита и молекулами растворителя. [22]
На самом же деле практически несжимаемыми являются ионы. В табл. XVI, 3 приводятся величины мольных объемов соли в кристаллическом состоянии f2 и кажущихся мольных объемов ij2 соли в водных растворах при бесконечном разбавлении. Разность этих величин i - - f2 равна изменению объема раствора при растворении 1 моль соли в бесконечно большом количестве воды. [23]
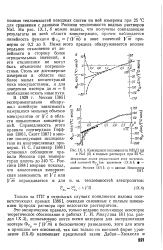 |
Кажущиеся теплоемкости МН4С1 ( а и Nal ( б в водных растворах при 25 СС. Штриховые линии ограничивают зону погрешностей значений Ф [ уравнение ]. . [24] |
Ниже этого предела обнаруживается вполне реальное отклонение от линейности в сторону более отрицательных значений, и эти отклонения не могут быть объяснены погрешностями. Столь же достоверные измерения в области еще более малых концентраций пока неосуществимы, и для доведения изотерм до т О необходимо искать иные пути. В 1929 г. Мессон [385] экспериментально обнаружил линейную зависимость кажущихся мольных объемов электролитов от УС в области повышенных концентраций. Справедливость этого правила подтвердили Гефф-кен [386], Скотт [387] и многие последующие исследователи на многочисленных примерах. Мессона при температурах вплоть до 340 С. [25]
Коэффициент В определяется взаимодействием ионов с растворителем, и величина его может быть как положительной, так и отрицательной в зависимости от свойств растворенного вещества и растворителя. Для водных растворов 1 - 1 электролитов, содержащих небольшие гидрофобные ионы, значения В обычно не превышают 0 2 л / моль; для солей с отрицательно гидратированными ионами В может принимать отрицательные значения: Й ( КС1, ag) - 0 014 л / моль, 5 ( CsNO3, ag) - 0 090 л / моль. Водные растворы электролитов с многовалентными или большими гидрофобными ионами, а также растворы солей в типичных неводных растворителях имеют сравнительно большие значения коэффи-циента В: B [ ( C4H9) H4NCl ag) 1 27 л / моль В ( КС1, DMSO) 0 80 л / моль. Необходимо отметить, что связь коэффициента В с различными макроскопическими параметрами широко используется для описания растворов электролитов. В работе [78] анализируется его связь с предельными кажущимися мольными объемами электролита: авторы [79] выводят уравнения, связывающие В с парциальными мольными объемами растворителя, электролита и с парциальными мольными свободными энтальпиями образования полости в растворе электролита и в растворителе. Наибольшее распространение для оценки ионных вкладов получили методы, основанные на электролитах сравнения, в качестве которых для водных растворов были использованы галогениды щелочных металлов, например, fi ( Rb) В ( Вг), а для неводных - iPe3BuNBPh4, Bu4NBPh4 и др. Однако получаемые результаты носят лишь оценочный характер, так как при этом исходят из предположения, что коэффициенты В характеризуют только взаимодействия ион-растворитель. [26]
Истинные и кажущиеся значения мольных объемов совпадают при бесконечном разбавлении. Именно эти полученные при экстраполяции объемы и будут здесь рассмотрены. Опытные данные показывают, что F2 для электролитов в воде может быть иногда отрицательным. При попытке разложить парциальный мольный объем электролита на ионные составляющие было выдвинуто [45] предположение о равенстве объемов ионов хлора и аммония. В связи с этим обращали внимание на тот факт, что кажущийся мольный объем этой соли приблизительно равен удвоенному мольному объему воды; он мало изменяется с температурой по сравнению с мольными объемами других электролитов. [27]
Страницы: 1 2