Молярный объем - вещество
Cтраница 2
Другая существенная особенность систем, состоящих из конденсированных фаз, заключается в том, что молярные объемы вещества в конденсированном состоянии при не очень высоких давлениях во много раз меньше, чем в паровой фазе, а изменение объема при смешении, как правило, невелико. Поэтому парциальные молярные объемы мало отличаются от молярных объемов чистых веществ при одинаковой температуре. [16]
В соотношение ( 5 - 41) параметрически входит уравнение состояния, из которого определяется молярный объем вещества V. [17]
При сравнении парахора различных соединений были получены данные, показывающие, какой вклад в общую величину молярного объема вещества вносят отдельные органические радикалы и структуры атомов. [18]
Из этого уравнения следует, что при постоянной температуре величина изменения содержания вещества в газовой среде от давления определяется разностью молярных объемов вещества в обеих фазах. [19]
Уравнение (8.9) ( уравнение Клапейрона - Клаузиуса) выражает зависимость между молярной теплотой фазового превращения, давлением, температурой и изменением молярного объема вещества. [20]
Все эти данные подтверждают справедливость допущения о том, что в достаточно хорошем приближении молярный объем адсорбированного вещества может быть заменен в большинстве случаев для адсорбционных расчетов молярным объемом вещества в жидком состоянии. [21]
Все эти данные подтверждают справедливость допущения о том, что в достаточно хорошем приближении молярный объем адсорбированного вещества может быть заменен в большинстве случаев для адсорбционных расчетов молярным объемом вещества в жидком состоянии. [22]
При этом только следует иметь в виду, что статистическая сумма каждого из компонентов реакции в общем случае содержит множитель V RT / P, где V - молярный объем вещества; Р - давление, предполагаемое постоянным ( ср. [23]
Так как в этом выражении M / D - d представляет собой молярный объем, зависящий, как известно, при постоянной температуре от строения вещества, то парахор дает возможность сравнивать молярные объемы веществ, не учитывая их зависимость от температуры. [24]
Левченко и Кожановым [161] было показано, что на форму изотермы адсорбции отдельных веществ на данном адсорбенте влияют не только значения уменьшения их стандартной молярной энергии Гиббса адсорбции - АС0, но также растворимость и молярный объем веществ. [25]
Левченко и Кожановым [161] было показано, что на форму изотермы адсорбции отдельных веществ на данном адсорбенте влияют не только значения уменьшения их стандартной молярной энергии Гиббса адсорбции - AG, но также растворимость и молярный объем веществ. Был проведен расчет изотерм адсорбции органических веществ из водных растворов и количественно выявлена роль перечисленных факторов. [26]
В работе [162] было исследовано влияние отношения количеств компонентов бинарной смеси в водном растворе до адсорбции Cos / Coi на форму парциальных изотерм адсорбции компонентов при условии равенства их молярных объемов и постоянства отношения % 2 / Ki, а также при постоянном ( эквимолярном) соотношении концентраций компонентов смеси в растворе до адсорбции, но при уменьшении соотношения молярных объемов веществ. Полученные результаты заслуживают более подробного рассмотрения. [27]
В работе [162] было исследовано влияние отношения количеств компонентов бинарной смеси в водном растворе до адсорбции С () 2 / Сщ на форму парциальных изотерм адсорбции компонентов при условии равенства их молярных объемов и постоянства отношения К 2 / К, а также при постоянном ( эквимолярном) соотношении концентраций компонентов смеси в растворе до адсорбции, но при уменьшении соотношения молярных объемов веществ. Полученные результаты заслуживают более подробного рассмотрения. [28]
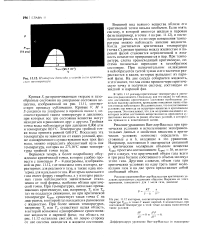 |
Иютермы диоксида углерода ii его критическая температура. [29] |
Решение уравнения Ван-дер - Ваальса при критических условиях и использование экспериментальных данных о свойствах вещества в критических условиях позволяет определить постоянные а и Ь, входящие в это уравнение. Например, постоянная b оказывается связанной с критическим молярным объемом вещества Кфит простым соотношением ККр т ЗЬ, из которого следует, что критический объем газа всего в три раза больше собственного объема молекул этого газа. Другими словами, объем газа при критических условиях на одну треть занят молекулами газа и на две трети представляет собой свободный объем. [30]
Страницы: 1 2 3