Собственный объем - молекула
Cтраница 1
Собственный объем молекул найдем, воспользовавшись поправкой Ван-дер - Ваальса, учитывающей силы отталкивания молекул и численно равной объему, который недоступен для молекул реального газа при их движении. [1]
Собственный объем молекулы обычно приравнивается объему, ограниченному замкнутой поверхностью, образованной при пересечении ван-дер-ваальсовых сфер отдельных атомов. Свободный объем - разность между объемом вещества и суммой собственных объемов содержащихся в нем молекул. [2]
Собственный объем молекул, рассчитанный из уравнения ван-дер - Ваальса, превышает величину V. Так, для гексана коэффициент Ь из уравнения ван-дер - Ваальса равен 0 007850, отсюда Ум 176 - 10 - ма / кмоль, в то время как V 130 5 - 10 - 8м / кмоль при 20 РС. [3]
Собственный объем молекул ничтожно мал по сравнению с объемом, занимаемым газом. Молекулы представляют собой маленькие сферы, не взаимодействующие друг с другом, за исключением момента столкновения. [4]
Собственный объем молекул также весьма мал по сравнению с объемом, приходящимся на межмолекулярные промежутки. Объем газа практически зависит от числа молекул, а также от температуры и давления, но не от химической природы молекул. Поэтому одинаковое число молекул различных газов занимает одинаковый объем при одинаковых условиях. При больших давлениях и очень низких температурах, когда межмолекулярные промежутки резко уменьшаются и приходится принимать во внимание объем самих молекул, возникают отступления от закона Авогадро. [5]
Определение собственного объема молекулы в жидкости, с которым связан первый вклад, в свою очередь, не может быть сделано однозначно. [6]
Учет собственного объема молекул и представление о молекулах в виде шариков, центры которых могут сближаться только до расстояния, равного их диаметру, по существу е сть простейший способ учета сил отталкивания между молекулами. [7]
Если собственным объемом молекул можно пренебречь ( Ь0), а учитывать только силы притяжения молекул ( поправка яй0), то при расширении газа, как указывалось выше, газ охлаждается. Но это означает, что наибольшее значение имеет отталкивание молекул. [8]
Следовательно, собственный объем молекул составляет 0 91 % от объема сосуда. [9]
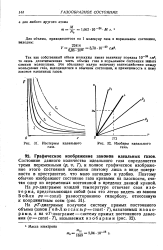 |
Изотермы идеального газа.| Изобары идеального газа. [10] |
Так как собственный объем молекулы имеет величину порядка 10 - 24 см3, то лишь десятитысячная часть объема газа в нормальном состоянии занята самими молекулами. Это объясняет малую величину взаимодействия между молекулами газа, находящегося в обычном состоянии, и применимость к нему законов идеальных газов. [11]
В действительности собственный объем молекул уменьшает свободное пространство для их движения. [12]
 |
Вязкость воды при разных температурах. [13] |
Ксобств - собственный объем молекул; WA - постоянная Авогадро; М - молекулярная масса; d - плотность; Т - температура; Е - энергия связи между молекулами жидкости. [14]
Если за собственный объем молекулы принять объем сферы радиусом гб / 2, то из (58.5) следует, что поправка b по Ван-дер - Ваальсу в четыре раза больше собственного объема молекул. [15]
Страницы: 1 2 3 4