Собственный объем - молекула
Cтраница 2
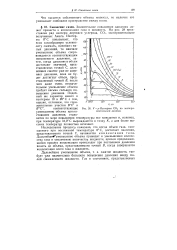 |
V - р - Изотермы СО2 по экспериментальным данным. [16] |
Что касается собственного объема молекул, то наличие его уменьшает свободное пространство между ними. [17]
Что касается собственного объема молекул, то наличие его уменьшает свободное пространство между ними и соответственно уменьшает длину свободного пути молекул. [18]
Что касается собственного объема молекул, то наличие его уменьшает свободное пространство между ними. [19]
Постоянная Ъ характеризует собственный объем молекул 1 моль вещества. Занимая часть пространства, в котором находится газ, молекулы уменьшают объем пространства, в котором они могли бы беспрепятственно перемещаться; это и отражается в уравнении Ван-дер - Ваальса вычитанием из объема, занимаемого газом, собственного объема молекул. [20]
Авогадро, со собственный объем молекул в расчете на 1 моль); ЕА, Ев, и ЕАв - соответственно энергия связи между молекулами А, В, л АВ. [21]
Член b учитывает собственный объем молекул. Для практических расчетов уравнение Ван-дер - Ваальса не рекомендуется использовать, так как результаты, полученные при расчете по формуле ( 2) отличаются от результатов, полученных опытным путем. [22]
 |
Газовая пипетка - прибор для отбора точного объема газа. [23] |
Поправка Ъ учитывает собственный объем молекул в общем объеме газа. Так как объем молекул идеального газа равен нулю, то измеренный объем реального газа несколько больше. [24]
Величина b учитывает собственный объем молекул и силы отталкивания между ними при малых расстояниях. [25]
Таким образом, общий собственный объем молекул 40 молей гелия, помещенного в сосуд емкостью 1 м3, составляет около 0 0001 объема сосуда. При этих условиях, очевидно, собственным объемом молекул можно пренебречь и считать, что молекулы двигаются практически во всем объеме сосуда. [26]
Вспомним, что собственный объем молекул газа составляет ничтожную часть от объема, занятого газом. Следовательно, молекулы идеального газа должны иметь пренебрежимо малые размеры. [27]
Оказывается, что собственный объем молекул пара практически всегда ничтожно мал по сравнению с объемом, занятым паром. Поэтому, если в пространстве находится пар какой-либо жидкости ( даже и насыщающий), то это не мешает испаряться в нем другой жидкости. Общее давление паров в этом случае равно сумме давлений паров обеих жидкостей. Это свойство паров выражается законом, открытым английским ученым А. Дальтоном: давление смеси паров и газов равно сумме давлений, создаваемых каждым из них в отдельности, если между ними нет химического взаимодействия. [28]
Объем b равен учетверенному собственному объему молекул. Если, например, в сосуде находятся две молекулы, то центр любой из них не может приблизиться к центру другой молекулы на расстояние, меньшее диаметра d молекулы. [29]
Объем Ь равен учетверенному собственному объему молекул. Если, например, в сосуде находятся две молекулы, то центр любой из них не может приблизиться к центру другой молекулы на расстояние, меньшее диаметра d молекулы. [30]
Страницы: 1 2 3 4