Бикарбонат - кальций
Cтраница 1
Бикарбонаты кальция и магния обусловливают карбонатную жесткость, а хлориды и сульфаты кальция и магния - некарбонатную жесткость. [1]
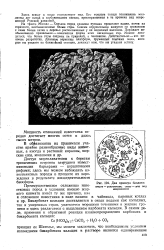 |
Два примера биолита. [2] |
Бикарбонат кальция доставляется в океан водами как холодных, так и умеренных стран, увлекается морскими течениями в жаркие тропики и здесь разлагается с выделением карбоната кальция. [3]
Бикарбонаты кальция и магния обусловливают карбонатную жесткость, а хлориды и сульфаты кальция и магния - некарбонатную жесткость. [4]
Бикарбонат кальция проявляет свои защитные свойства в агрессивной среде только в присутствии растворенного кислорода. В результате коррозии, идущей с кислородной деполяризацией, происходит защелачивание среды у катодных участков металла, что ведет к осаждению карбоната кальция вместе со ржавчиной. Образующийся в этих условиях плотный слой осадков, состоящий на 65 - 75 % из СаСО3 и на 20 - 25 % из окислов железа, обладает высокой адгезией и проявляет повышенные защитные свойства, затрудняя дальнейшую диффузию кислорода к поверхности металла. [5]
Бикарбонаты кальция и магния Са ( НСОзЬ и Mg ( HCOs) 2, называются солями карбонатной жесткости. Сульфаты и хлориды кальция и магния CaSO4, MgSC4, СаС12 и MgCb называются солями постоянной жесткости. [6]
Бикарбонаты кальция и магния сравнительно легко растворимы. [7]
Бикарбонаты кальция и магния Са ( НСОзЬ и Mg ( HCO3) 2, называются солями карбонатной жесткости. Сульфаты и хлориды кальция и магния CaSO4, MgSO4, СаС12 и MgCl2 называются солями постоянной жесткости. [8]
Бикарбонат кальция выносится в окружающую среду, а карбонат кальция выпадает в осадок и затем растворяется вновь поступающей угольной кислотой. [9]
Бикарбонаты кальция и магния обусловливают карбонатную жесткость. При нагревании воды растворенные бикарбонаты разлагаются и карбонатная жесткость при этом сильно снижается. Полного устранения карбонатной жесткости не происходит вследствие того, что карбонат кальция и особенно магния, несколько растворим в воде. [10]
Бикарбонат кальция при нагревании разлагается с образованием средней соли, двуокиси углерода и воды. [11]
Бикарбонат кальция при нагревании разлагается, причем образуются средняя соль, углекислый газ и вода. [12]
Бикарбонат кальция наряду с бикарбонатом магния обусловливает временную жесткость воды. Жесткость воды выражается в градусах ( старая единица) и в миллиграмм-эквивалентах на 1 л воды ( новая единица) ( см. примечание стр. [13]
Бикарбонаты кальция и магния сравнительно с их карбонатами отличаются большей растворимостью в воде. Например, Са ( НСОзЬ при 4 растворяется в количестве 62 мг в 1 л, между тем как СаСОз при тех же условиях растворяется в количестве лишь 11 мг в 1 л воды. [14]
Бикарбонат кальция наряду с бикарбонатом магния обусловливает временную жесткость воды. [15]
Страницы: 1 2 3 4