Бикарбонат - натрий
Cтраница 1
Бикарбонат натрия ( кисльш углекислый натрий, питьевая сода) NaHCOs - белое вещество, обычно порошкообразное. Это соединение применяют в кулинарии, медицине и для производства пекарского порошка. [1]
Бикарбонат натрия NaHC03 ( двууглекислый натрий, питьевая сода) - мелкий белый порошок. В воде значительно менее растворим, чем карбонат натрия. [2]
Бикарбонат натрия, 5 % - ный раствор, содержащий 20 % хлорида натрия. [3]
Бикарбонат натрия, 5 % - ный раствор, содержащий 20 % хлорида натрия; Уксусная кислота. [4]
Бикарбонат натрия ( ГОСТ 2156 - 52) - сода двууглекислая, сода питьевая - кристаллический порошок белого цвета NaHCO3, растворяется в воде и не растворяется в этиловом спирте. Выпускается двух марок: технический и медицинский. Получается как полупродукт в производстве кальцинированной соды. [5]
Бикарбонат натрия нейтрализует кислые продукты, поступающие в организм или накапливающиеся в нем в результате нарушения обмена веществ. [6]
Бикарбонат натрия затем легко, если нужно, превратить в карбонат нагреванием. Нашатырь не-выбрасывается, а используется для регенерации из него аммиака при помощи негаше-яой извести. [7]
Бикарбонат натрия ( ГОСТ В-2156-43) бывает трех сортов: А, Б и В. [8]
Бикарбонат натрия, 4 % - ный раствор, к 1 л которого прибавлено несколько капель концентрированной соляной кислоты. [9]
Бикарбонат натрия NaHCO3 представляет собой белый кри сталлический порошок, растворимый в воде. При взаимодействии с кислотами и при нагревании он разлагается с выделением двуокиси углерода. [10]
Бикарбонат натрия NaHCO3 представляет собой белый кристаллический порошок, растворимый в воде. При взаимодействии с кислотами и при нагревании он разлагается с выделением двуокиси углерода. [11]
Бикарбонат натрия, полученный таким образом, естественно, пропитан маточным раствором. [12]
Бикарбонат натрия получают, вводя двуокись углерода в раствор карбоната натрия. При этом стремятся получать частицы размером менее 0 1 мм. Это достигают двумя способами: просеиванием или измельчением. [13]
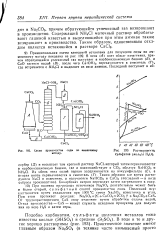 |
Схема произродства соды по аммиачному. [14] |
Бикарбонат натрия переводят затем нагреванием в соду. При наличии природных источников NajSO, рентабельным может быть и более старый, сульфатный способ производства соды. Последний осуществляется путем сплавления при 1000 С смеси Na2SO4, известняка и угля. От труднорастворимого CaS соду отделяют путем обработки сплава водой. Отход производства - CaS - может служить исходным продуктом для получения из него H2S и затем серы. [15]
Страницы: 1 2 3 4