Окисел - железо
Cтраница 2
 |
Схема технологического процесса извлечения окиси железа и соляной кислоты из отходов травильного раствора ( процесс Лурги. [16] |
Образование именно этого окисла железа Ре2Оз, а не Fe ( OH) 2 или Fe ( OH) 3 обусловлено определенными условиями реакции, значением величины рН среды и температуры. Детальное рассмотрение этого вопроса выходит за рамки настоящей книги. Читателям, которые не стремятся расширить свои познания в этой области, следует напомнить, что знающий специалист по промышленной химии или квалифицированный инженер-химик может существенным образом способствовать делу защиты окружающей среды от загрязнения. [17]
 |
Распыление газопоглотителя. [18] |
Прибавление к сплаву альба окисла железа Fe2O3 и порошка титана и тория ( газопоглотители бати и бато) позволяет распылять их при низких температурах полочки ( около 900qC), когда никель практически не распыляется. [19]
Добавки соды затягивают процесс восстановления окисла железа, а поташа - ускоряют. [20]
Термитную смесь, состоящую из измельченного окисла железа и металлического алюминия, засыпают в форму, окружающую присоединяемый к трубе стержень из круглой стали. После установки формы и заполнения ее термитной смесью производится возбуждение термитной реакции местным ее нагревом до температуры не менее 1000 С. Для этой цели применяются обычно термитные спички. [21]
Термитную смесь, состоящую из измельченного окисла железа и металлического алюминия, засыпают в форму, окружающую присоединяемый к трубе стержень из круглой стали. После установки формы и заполнения ее термитной смесью производится возбуждение термитной реакцир. Для этой цели применяются обычно термитные спички. [22]
Таким образом, вновь регенерируется гидрат окисла железа. Однако регенерация не избавляет от накопления в очистной массе свободной серы. Когда содержание серы достигнет 40 - 50 %, поглотительная способность массы резко снижается, и ее нужно выгружать и заменять свежей. Отходы от очистки могут служить сырьем в производстве серной кислоты. [23]
Конечным результатом будет матрица окалины из окисла железа, содержащая катионы никеля с малыми островками никеля, и металлический слой у поверхности раздела, обогащенной никелем ( фиг. Присутствие никеля может тормозить дальнейшее окисление. Механизм этого эффекта строится не на формировании окалины поверх первоначальной поверхности металла. Он, по-видимому, сводится к внутренней диффузии анионов, которая сопровождается восстановлением окисленного никеля. При этом возможны разные формы существования никеля - от цепочки островков до тонкой непрерывной ажурной структуры. [24]
В результате воздействия кислорода на детали образуется окисел железа FeO. Этот окисел производит обезуглероживание: он забирает с поверхности деталей углерод, который соединяется с кислородом, образуя уже знакомую нам окись углерода СО. Чтобы избежать разъедания, на поверхность разогретой ванны забрасывают мелкодробленый древесный уголь, который не допускает растворения кислорода воздуха в ванне. С этой целью в разогретую ванну забрасывают толченый ферросилиций ( 1 % от веса соли в ванне), который связывает окисел железа в шлак, оседающий на дно ванны. [25]
Если же железо в атмосфере водяных паров или окисел железа в атмосфере водорода нагреваются в закрытом сосуде ( при избытке железа или его окисла), реакция идет до тех пор, пока не установится отвечающее данной температуре равновесие. [26]
Если же железо в атмосфере водяных паров или окисел железа в атмосфере водорода нагреваются в закрытом сосуде ( при избытке железа или его окисла), реакция идет до тех пор, пока не установится отвечающее данной температуре равновесие. [27]
У железистого асбеста, содержащего до 8 % окисла железа, fv Ю5 - 10е ом см. Из нитей железистого асбеста изготовляют полупроводящие ленты, применяемые для выравнивания электрического поля на поверхности обмоток электрических машин высокого напряжения. [28]
Появление цветов побежалости связано с интерференцией света в пленках окисла железа, возникающих на поверхности детали при нагревании. Для углеродистых сталей в интервале температур 220 - 300 С различают следующие цвета побежалости: при температуре 220 - 240 С - соломенно-желтый; при 240 - 260 С - оранжевый; при 260 - 280 С - красно-фиолетовый; при 280 - 300 С - синий. Контроль температуры отпуска по цветам побежалости приближенный и требует от исполнителя навыка, приобретенного опытом работы. [29]
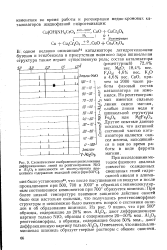 |
Схематическое изображение расположения диффракционных линий на рентгенограммах NiO и А1аО3 в зависимости от молекулярного процентного содержания исходной смеси ( при 500 С. [30] |
Страницы: 1 2 3 4