Чистый окисел
Cтраница 1
Чистый окисел V2O5 является полупроводником не только в твердом, но и в жидком состоянии и обладает электронной проводимостью. Стекла, синтезированные на основе V2Os и Р2Оз, также относятся к числу типичных полупроводников ( стр. Однако, находясь в силикатных стеклах в ограниченных количествах, окисел V2O5 теряет электронную проводимость. Например, проводимость стекол состава ( 15 - 25) Na2O - ( 10 - 15) VO2 5 - ( 60 - 75) SiO2, по синтезу, имеет чисто ионный характер, по крайней мере при 200 - 350 и замена SiO2 на VO2 s повышает электросопротивление стекол. Вместе с тем, частичное восстановление V2O5 до V2O4 ведет к снижению сопротивления на 1 5 - 2 порядка. [1]
Если шлак, кроме чистого окисла кремния, содержит окислы металлов, то эти окислы разрушают четырехвалентную связь. В пространственной структуре посторонние окислы располагаются в углах четырехвалентной связи и вызывают большую легкоплавкость окисла кремния в присутствии окислов металлов. [2]
Фазовый состав изменяется от чистого соединения до чистого окисла или смеси окиси с остатками неразложенного исходного вещества. Во второй области в интервале температур от Т до Т2 химический состав изменяется мало, здесь происходит доразложение исходного соединения и рекристаллизация образовавшегося окисла. Уменьшение величины поверхности и, следовательно, увеличение размеров частиц ( элементов структуры), образующих ее, могут быть обусловлены следующими процессами: парофазным переносом вещества, благодаря образованию летучих соединений при взаимодействии окисла с окружающей средой или продуктом разложения исходного вещества ( примером является взаимодействие SiO2 и водяного пара с образованием Si ( OH) 4); миграцией молекул по поверхности; объемной диффузией и вязким течением. Соотношение скоростей этих процессов зависит как от химической природы окислов, так и от условий термической обработки. [3]
Используемая в технике керамика в своей основе имеет либо чистый окисел алюминия, и тогда она пригодна для работ при температурах 1000 С и выше, либо наряду с окислом алюминия имеет стеклофазу и в этом случае эксплуатационная температура не превышает 500 - 600 С. [4]
Возгонка и испарение из расплава MoO s применяются для получения чистого окисла. Значительное влияние на возгонку МоО3 оказывают примеси. Эти соединения растворяются в расплаве МоО3, понижая упругость его пара. Упругость пара молибдатов повышается с температурой, и перенос примеси увеличивается. Так, давление пара РЬМоО4 при 1016 0 08, при 1060 0 23 мм рт. ст. В процессе возгонки к порошку МоО 3 добавляют кварц, облегчающий разгрузку невозогнанного остатка. В противном случае остаток МоО3 налипает на под и пропитывает его. [5]
Следует отметить, что открытие новой области применения того или иного чистого окисла или соединения неизбежно приводит к получению дополнительного количества соединений других РЗМ. Перспективы использования РЗМ в производстве чугуна, стали и цветных металлов оцениваются в настоящее время как исключительно благоприятные. [6]
Прежде всего следует выяснить, чем вообще определяется величина удельной поверхности чистого окисла. Общеизвестно, что величина удельной поверхности зависит от метода и условий получения окисла. Если окисел получается путем целого ряда последовательных операций, то условия проведения каждой операции в той или иной степени влияют на величину поверхности конечного продукта. Значительно реже обращают внимание на то, что величина удельной поверхности зависит от природы самого окисла. При одинаковых условиях получения различные окислы имеют разные величины удельной поверхности. [7]
Пока нет возможности предсказать, какую величину поверхности должна иметь фаза чистого окисла или соединения, состоящего из двух окислов. Можно, однако, попытаться ответить на более простой вопрос: будет ли наблюдаться увеличение удельной поверхности окисла при растворении в нем другого окисла. Ответ на этот вопрос достаточно важен, так как образование твердых растворов - очень распространенное явление для смешанных окисных катализаторов. [8]
Из рассмотрения особенностей окисления сплавов системы медь - никель вытекает, что область концентраций, в которой образуется чистый окисел менее благородного металла, существенным образом зависит от разности упругостей диссоциации окислов сплавообразующих металлов или от разности свободных энергий образования этих окислов. [9]
В медных сплавах, в состав которых входят более благородные металлы, окисная пленка будет состоять в основном из чистого окисла меди, так как окислы более благородных металлов имеют более высокие давления, диссоциации. [10]
Допустим, что мы нагреваем чистый образец двуокиси марганца МпОг весом 0 435 г. При этой реакции выделяется только кислород и образуется 0 382 г другого чистого окисла. [11]
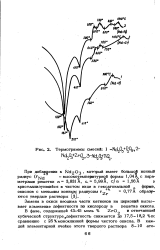 |
Термограммы смесей. 1. [12] |
В фазе, содержащей 43 - 45 моль % ZrO и отвечающей кубической структуре дефектность снижается до 17 5 - 18 2 % пс сравнению с 25 % моноклинной формы чистого окисла. [13]
Сульфид состава Cr7S8 ( CrSliU) окисляется аналогично, по с более медленным присоединением кислорода, рентгенографический анализ обнаруживает появление Сг3О3 начиная с температуры 650 С, вокруг зерен сульфида образуется защитный слой окисла, который затрудняет диффузию кислорода и объясняет присутствие кислорода при высоких температурах. Чистый окисел Сг2О3 образуется при температуре 1000 С. [14]
Основные залежи его находятся в СССР, а также в США и в Бразилии. Высокая температура плавления для чистого окисла, равная 2687 20 [43] ( по другим данным [44] - выше3000), с одной стороны, и малый коэффициент расширения и высокая термическая стойкость - с другой, заставляют в некоторых случаях предпочесть окись циркония магнезии. Плавка, так же, как для магнезии, повышает качество ZrOa. Плавленую окись циркония, а также природный минерал циркон применяют в качестве добавок к массе для изготовления муллитовых, магнезитовых и других кирпичей с целью повышения их теплостойкости. [15]
Страницы: 1 2