Чистый окисел
Cтраница 2
Наиболее убедительным доказательством зависимости энергии активации от материала контактов могут служить значения энергии активации, полученные для термисторов с одинаковым составом полупроводящего вещества, электроды которых изготовлены из различных металлов. Поэтому нами были определены значения энергии активации термисторов из химически чистого окисла меди СиО, одни из которых были изготовлены без металлических электродов, другие - с электродами из меди, третьи - с электродами из цинка. [16]
В 1931 г. был предложен в Германии фирмой Сименс и Гальске для изготовления свечных изоляторов новый материал-плотная масса из кристаллов чистого окисла алюминия. Эта масса обладает большой термич. Теплопроводность этих масс примерно в 20 раз больше, чем у керамиковых материалов. При применении этого материала, обладающего большой теплопроводностью, имеется возможность создать изолятор с удлиненной нижней частью, благодаря чему путь для утечки тока, получающийся при осаждении на изоляторе нагара, увеличивается, и надежность действия С. [17]
Сернистая кислота мгновенно превращает двуокись свинца ( Pb) в сернокислый свинец. Чтобы получить необходимое нам число, нужно знать количество тепла, которое выделяется при соединении окиси свинца с серной кислотой, а также количество тепла, которое выделяет второй атом кислорода при образовании чистого окисла. Первую величину не особенно трудно определить, а для второй - я не знаю способов определения. Я пытался пойти по другому пути, а именно: по пути сжигания смеси водорода и сернистой кислоты в атмосфере кислорода. [18]
С, свидетельствуют о том, что си-лан плохо смачивается смолами и водой. Из результатов исследований, проведенных Баском [6] и Ли [58], также следует, что при адсорбции юилановых аппретов на ( поверхностях с высокой энергией, таких, как стекло, корунд и сталь ( табл. 14), их критическое поверхностное натяжение уменьшается до ( 254 - 45) - 10 - 5 Н / см. Эта величина значительно ниже YC чистого окисла или металлической поверхности. [19]
Исходя из представлений о механизме окисления, разрабатываются составы сплавов, стойких к воздействию кислорода при повышенных температурах. Такие сплавы называются жаростойкими, основой их являются железо, никель медь. На поверхности жаростойких сплавов возникает защитный слой, состоящий либо из чистого окисла добавленного легирующего компонента, либо из сложного окисла основы и легирующего компонента. Скорость окисления ( газовой коррозии) при этом уменьшается в десятки раз в сравнении с окислением чистой основы. [20]
Окислы-силикаты и чистые окислы материалов. Для металлов, легко загрязняемых кремнием, идеальным огнеупорным материалом обычно являются чистые тугоплавкие окислы, которые не взаимодействуют с расплавом. Тигли из чистых окислов, однако, трудно изготовить, так как частицы порошка чистого окисла плохо связываются при температурах более низких, чем температура спекания, а механические свойства спеченных окислов очень низки. [21]
Окислы-силикаты и чистые окислы материалов. Для металлов, легко загрязняемых кремнием, идеальным огнеупорным материалом обычно являются чистые тугоплавкие окислы, которые не взаимодействуют с расплавом. Тигли из чистых окислов, однако, трудно изготовить, так как частицы порошка чистого окисла плохо связываются при температурах более низких, чем температура спекания, а механические свойства спеченных окислов очень низки. [22]
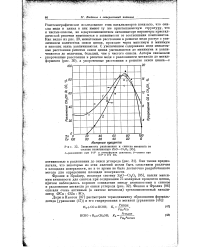 |
Зависимость разложения и синтеза метанола от состава катализатора ZnO - Сг20я. [23] |
Рентгенографическое исследование этих катализаторов показало, что окислы меди и цинка в них имеют ту же кристаллическую структуру, что и чистые окислы, но в двухкомпонентном катализаторе параметры кристаллической решетки изменяются в зависимости от соотношения компонентов. Как видно из рис. 29, межатомные расстояния в решетке меди растут с увеличением количества окиси цинка, проходят через максимум и минимум и наконец опять увеличиваются. С увеличением содержания меди межатомные расстояния решетки окиси цинка уменьшаются до минимума и увеличиваются до величины, большей, чем у чистого окисла. [24]
Окись кобальта ( П) ( вещество оливково-зеленого цвета) легко можно получить взаимодействием металла с кислородом при высокой температуре, а также пиролизом карбоната или нитрата и многими другими способами. Окись кобальта ( П) имеет структуру каменной соли и при обычной температуре антиферромагнитна. Он представляет собой простую шпинель, в которой ионы Со занимают тетраэдрические пустоты, а диамагнитные ионы Со111 - октаэдрические. Существование чистого окисла Со2О3 до сих пор не доказано. [25]
Различные окислы спекаются при разной температуре. В некоторых случаях она близка к температуре плавления окисла. Труд-носпекаемыс окислы получают в виде плотной керамики после двухкратного обжпга. Для этого спеченный образец тщательно растирают в фарфоровой ступке, прессуют п подвергают вторичному обжигу. В тех случаях, когда чистый окисел не спекается, или для его спекания требуется слишком высокая температура, к нему добавляют в незначительном количестве плавень, образующий па гранях кристаллов легкоплавкие соединения с исходным окислом, что п обеспечивает цементацию. [26]
Для наружной изоляции и внешней защиты применяют иногда и пластич. В 1931 г. был предложен в Германии фирмой Сименс и Гальске для изготовления свечных изоляторов новый материал-плотная масса из кристаллов чистого окисла алюминия. Эта масса обладает большой термич. Теплопроводность этих масс примерно в 20 раз больше, чем у керамиковых материалов. При применении этого материала, обладающего большой теплопроводностью, имеется возможность создать изолятор с удлиненной нижней частью, благодаря чему путь для утечки тока, получающийся при осаждении на изоляторе нагара, увеличивается, и надежность действия С. [27]
Страницы: 1 2