Окисление - индикатор
Cтраница 3
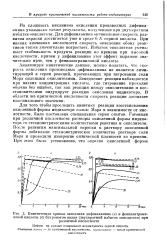 |
Кинетические кривые окисления дифениламина ( а и фенилантраниловой кислоты ( б бпхроматом калия ( двухкратный избыток окислителя при. [31] |
Анализируя кинетические данные, можно полагать, что скорость окисления производных дифениламина не является лимитирующей в серии реакций, протекающих при титровании соли Мора сильными окислителями. Замедление реакции наблюдается при низких концентрациях кислоты, где титрование проходит обычно без ошибок, так как реакция между окислителями и восстановителями индуцирует реакцию окисления индикатора. В области же критической кислотности скорость реакции достигает максимального значения. [32]
Такой же объем воды помещают в колбу для проведения контрольного опыта. Важно, чтобы в колбах с анализируемой и контрольной пробами количество индикатора было одинаковым, поскольку на следующем этапе анализа происходит незначительное, но поддающееся измерению окисление индикатора. [33]
Потенциалы систем в случае растворимости окисленной и восстановленной форм индикатора можно определить после того, как установлено, какие окислители и восстановители способны превращать индикатор из одного состояния окисления в другое. Обычно принимается, что между двумя состояниями индикатора ( с различными степенями окисления) и окислительно-восстановительной буферной системой устанавливается равновесие и что условия опыта по определению степени окисления индикатора ( например, соосаждение одной, но не другой формы) не вызывают сдвига равновесия. [34]
При исследовании поведения свободных от носителя индикаторов иногда можно получить некоторые данные, указывающие на состояние окисления индикатора, но такие данные редко являются надежными. Например, изоморфное внедрение индикатора в осадок указывает на то, что заряд, размер и координационное число для ионов носителя и индикатора одинаковы, и это дает возможность определить вероятное состояние окисления индикатора. [35]
Меркурометрический анализ бромид - и хлорид-ионов в широком интервале концентраций ( 0 005 - 0 5 N) осуществляется с индикацией КТТ по изменению окраски вариаминового синего [513], обратимо окисляющегося небольшим избытком Hg ( I) при рН 2 - 6 в продукт фиолетового цвета. Титрование рекомендуется вести при 50 С, вводя на каждые 10 мл, анализируемого раствора по 0 5мл 0 1 % - ного раствора вариаминового синего и по 1 г твердого NH4N03, ускоряющего окисление индикатора. [36]
Индикаторы хромогенчерный ЕТ-00 и кислотный хро. Это обесцвечивание в литературе иногда объясняют тем, что в щелочной среде марганец ( - f - 2) очень легко окисляется кислородом воздуха до более высоких валентностей, а образовавшийся трех - или четырехвалентный марганец окисляет далее хромовый индикатор, вызывая его обесцвечивание. Наблюдение за скоростью окисления индикаторов в щелочной среде сильными окислителями, необратимость этого окисления и возвращение окраски индикаторов, обесцвеченных в присутствии солей марганца путем добавления гидроксиламина или гидразина, приводит нас к выводу, что обесцвечивание индикаторов в этом случае объясняется не разрушением его, а адсорбцией индикаторов на труднорастворимых гидроокисях трех - или четырехвалентного марганца. Введение в этот раствор восстановителя приводит к десорбции индикатора и возвращению его окраски. [37]
Указано возможное изменение степени окисления индикатора. Хотя начальная и конечная степени окисления индикатора часто окончательно не установлены, обычно можно на основании данных о химических свойствах сделать вывод о наиболее вероятной реакции. Для каждого элемента сначала указывается реакция восстановления, а затем - реакция окисления. [38]
В конечной точке избыточная капля раствора бромата реагирует с образующимся при реакции бромидом с выделением брома, который окрашивает раствор в желтый цвет. Значительно лучше и точнее титровать в присутствии метилоранжа, красная окраска которого в кислой среде исчезает от небольшого избытка бромата. При вычислении учитывают объем титрованного раствора КВгОз, расходуемый только на окисление индикатора. [39]
Дифениламин является очень чувствительным индикатором для определения точки эквивалентности при реакции ванадиевой кислоты с сульфатом железа ( II) в растворах, содержащих соляную или серную кислоту и [ если присутствует железо ( III) ] фосфорную кислоту. Железо ( III), мышьяк ( V) и уран ( VI) не влияют на определение. При титровании необходимо вводить небольшую поправку на то количество ванадиевой кислоты, которое расходуется на окисление индикатора. [40]
Реакция идет в нейтральном или слабокислом растворе, но не в щелочном или аммиачном, так как в первом Zn образует цинкат, а во втором-аммиакат. В качестве индикатора применяют дифениламин, который легко окисляется феррицианидом калия в азокраситель фиолетового цвета. Так как титрованным раствором является ферроцианид, то перед титрованием индикатор окисляют действием феррицианида, прибавляя последний к испытуемому раствору вместе с индикатором. Вследствие окисления индикатора раствор приобретает фиолетовую окраску. Как только все ионы цинка будут осаждены, первые капли K4 [ Fe ( CN) e ] будут взаимодействовать с индикатором, восстанавливая азокраситель в бесцветное соединение. Исчезновение фиолетовой окраски и указывает конец титрования. Надо иметь в виду, что осадок K2Zns [ Fe ( CN) e ] 2 белый с желто-зеленоватым оттенком, и потому нельзя ожидать обесцвечивания раствора с осадком. Так как в начале титрования был прибавлен окислитель K3 [ Fe ( CN) 6 ], то в конце титрования надо его восстановить добавкой избытка ферроцианида, являющегося восстановителем. Объем раствора восстановителя должен быть в полтора раза больше объема прибавленного окислителя, при равных их концентрациях. [41]
Реакция идет в нейтральном или слабокислом растворе, но не в щелочном или аммиачном, так как в первом Zn образует цинкат, а во втором - аммиакат. В качестве индикатора применяют дифениламин, который легко окисляется феррицианидом калия в азокраситель фиолетового цвета. Так как титрованным раствором является ферроцианид, то перед титрованием индикатор окисляют действием феррицианида, прибавляя последний к испытуемому раствору вместе с индикатором. Вследствие окисления индикатора раствор приобретает фиолетовую окраску. Как только все ионы цинка будут осаждены, первые капли K4lFe ( CN) 6 ] будут взаимодействовать с индикатором, восстанавливая азокраситель в бесцветное соединение. [42]
Анализируемый стандартный раствор иридия помещают в кварцевую пробирку 152 4 X 19 мм и добавляют 5 капель смеси серной кислоты и сульфата лития, 2 капли 72 % - ной хлорной кислоты и 1 каплю 3 3 -дихлорбензидина. Обмывают стенки пробирки водой и кипятят, чтобы сконцентрировать кислоту. Продолжают нагревать пробирку на верхней части пламени ( высотой 6 см), наблюдая за изменением окраски. Вследствие окисления индикатора раствор становится желтым, затем коричневым и, наконец, бледнеет. После исчезновения окраски нагревают еще 2 сек. Пробирку немедленно вынимают из пламени и вращают в почти горизонтальном положении, чтобы горячая кислота покрыла ее стенки примерно наполовину. Охлаждают, добавляют 2 мл воды, снова нагревают и слабо кипятят 10 сек, чтобы удалить хлор и двуокись хлора. Затем охлаждают и титруют раствором гидрохинона до почти полного исчезновения розово-фиолетовой окраски. Прибавляют 1 каплю индикатора и оставляют на 1 мин. За это время раствор становится желтым. Титрование продолжают до исчезновения желтой окраски. Затем раствор кипятят, снова окисляют, как описано выше, и вновь титруют гидрохиноном. [43]
Необратимые индикаторы - это соединения, которые разрушаются при введении избыто реагента и цвет которых не восстанавливается от дополнительного прибавления раствора определяемого вещества. Тот же метиловый оранжевый может быть примером необратимого индикатора в реакциях окисления - восстановления. Трехвалентную сурьму тигруют раствором бромата калия с метиловым оранжевым, до тех пор, пока в растворе нет избытка окислителя, индикатор окрашен в красный цвет. После точки эквивалентности некоторое количество растюра бромата калия приводит к окислению индикатора, вследствие чего раствор обесцвечивается. Естественно, что после прибавления раствора трехвалентной срьмы окраска не восстанавливается, так как весь индикатор разрушен. Необратимые индикаторы менее добны и применяются редко. [44]
Для определения конца титрования пользуются растворами метилоранжевого, метилкрасного, индигокармина и других интенсивно окрашенных веществ, которые обесцвечиваются вследствие окисления избытком бромата. Перед концом титрования окраска раствора немного бледнеет, так как местный избыток бромата постепенно разрушает часть индикатора. Для уверенности в правильном определении конца реакции необходимо перед окончанием титрования добавить еще 1 каплю раствора индикатора. В контрольной пробе определяют объем раствора КВгО3, уходящий только на окисление индикатора. [45]
Страницы: 1 2 3 4