Окисление - ион - хлор
Cтраница 2
Из литературы [2] известно, что растворение окисных руд в соляной кислоте протекает с выделением газообразного хлора за счет окисления ионов хлора окислами марганца ( MnOg, MngOg), при этом образуются кислые, богатые примесями растворы. [16]
На участке III потенциал достигает таких значений, что начинается разряд ионов хлора, адсорбция атомов хлора на электроде и практически весь ток расходуется на протекание электрохимической реакции окисления ионов хлора. [17]
На участке III потенциал достигает таких значений, что начинается разряд ионов хлора, адсорбция атомов хлора на электроде, и практически весь ток расходуется на протекание электрохимической реакции окисления ионов хлора. [19]
Можно применять р-ры, насыщенные газообразным хлором. Для повышения электропроводности электрохимия, окисление ионов хлора целесообразно проводить на фоне конц. [20]
В большинстве случаев электролизу подвергается раствор поваренной соли или хлористого калия. При этом на аноде происходит окисление ионов хлора с образованием молекулярного хлора. Однако Р условиях электросинтеза хлората этот хлор не выделяется из электролизера, а взаимодействует со щелочью, одновременно образующейся в эквивалентном количестве у катода. [21]
В последнем случае имеется дополнительная электрохимическая стадия окисления иона хлора и, кроме того, раствор больше загрязнен примесями, в частности хлорноватой кислотой, которая препятствует получению в дальнейшем перхлоратов. При большей или меньшей концентрации соляной кислоты, а также при меньшей анодной плотности выход по току резко уменьшается. [22]
Уменьшаются выходы по току и при сильном подкислении раствора. В значительной степени это объясняется расходом части тока на окисление ионов хлора, вводимых в раствор в виде соляной кислоты. [23]
Чаще всего для подкисления применяют серную кислоту. Соляная кислота менее пригодна для этой цели, так как при этом возможно окисление ионов хлора перманганатом или различными промежуточными окислами, образующимися при основной реакции. Поэтому солянокислые растворы используют только в том случае, если это необходимо для переведения в раствор анализируемого материала. Азотная кислота, особенно содержащая примеси окислов азота, неприменима потому, что она может вызывать ряд побочных процессов. [24]
Чаще всего для подкисЛения применяют серную кислоту. Соляная кислота менее пригодна для этой цели, так как при этом возможно окисление ионов хлора перманганатом или различными промежуточными окислами, образующимися при основной реакции. Поэтому солянокислые растворы используют только в том случае, если это необходимо для переведения в раствор анализируемого материала. Азотная кислота, особенно содержащая примеси окислов азота, неприменима потому, что она может вызывать ряд побочных процессов. [25]
В соляной кислоте при анодной поляризации QHK электродов изменяется мало, а ток расходуется на окисление ионов хлора. Потенциалы приведены относительно нормального водородного электрода. [26]
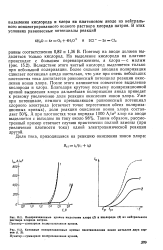 |
Поляризационные кривые выделения хлора ( / и кислорода ( 2 из нейтрального раствора хлорида натрия.| Катодные поляризационные кривые восстановления ионов металлов двух сортов ( /, 2. [27] |
Поэтому на аноде должен выделяться только кислород. Вследствие этого чистый кислород выделяется только при небольшой поляризации. Более сильная анодная поляризация сдвигает потенциал анода настолько, что уже при очень небольших плотностях тока достигается равновесный потенциал реакции окисления ионов хлора. После этого начинается совместное выделение кислорода и хлора. [28]
Для уменьшения затрат, связанных с очисткой хлорной кислоты от ионов хлора, обычно применяют каскад электролизеров. При этом весь процесс окисления с получением хлорной кислоты осуществляют в две стадии. На первой, продукционной, стадии электролиз ведут при оптимальном значении концентрации НС1 или растворенного в электролите хлора и при высоком значении выхода хлорной кислоты по току. На второй, так н & зы-ваемой очистной, стадии прекращают подачу соляной кислоты, HCI или СЬ в электролит и ведут окисление ионов хлора до остаточного содержания, определяемого требованиями потребителя хлорной кислоты. [29]
Страницы: 1 2
