Окисление - соляная кислота
Cтраница 1
Окисление соляной кислоты двуокисью свинца Выполнение работы: в пробирку внести один микрошпатель порошка двуокиси свинца и 3 - 4 капли концентрированной соляной кислоты уд. [1]
В лабораторных условиях хлор получается окислением соляной кислоты ( водный раствор хлористого водорода) двуокисью марганца МпО2: МпО3 4НС1 С12 МпС12 - f - 2ri O. В промышленности используется хлор, выделяющийся при электролизе хлористого натрия для получения едкого натра. С водородом хлор дает только одно соединение - хлористый водород НС1, водный раствор которого ( растворимость 42 г в 100 г раствора при давлении 1 am и 20) называется соляной кислотой, являющейся сильной кислотой, находящей широкое применение в технике. [2]
В лаборатории хлор обычно получают окислением соляной кислоты или ее солей различными окислителями ( MnO2, KMnOi, КзС О. В большинстве случаев окисляют НС1 или NaCl, В случае NaCl ( или других хлоридов) окисление производят в присутствии серной кислоты, образующей с хлоридами в растворе соляную кислоту, которая и взаимодействует с окислителем с образованием хлора. [3]
Напишите уравнение реакции получения хлора окислением соляной кислоты перманганатом калия, учитывая, что окислительное число марганца изменяется от 7 до 2 с образованием дихлорида марганца. [4]
Получаются галогены по типу получения хлора - окислением соляной кислоты или ее солей сильными окислителями: двуокисью марганца, перманганатом калия или бихроматом калия. [5]
Этот метод предусматривает получение хлорной кислоты электрохимиче - ким окислением соляной кислоты или хлора в концентрированных растворах хлорной кислоты. Хлорную кислоту очищают от примесей соляной кислоты электрохимически или термической отгонкой. [6]
Ист В 1772 г. Шееле получил первый из галогенов - хлор окислением соляной кислоты пиролюзитом. [7]
Усилия многих исследователей XIX столетия были направлены на утилизацию двуокиси марганца путем многократного использования ее в процессе окисления соляной кислоты. [8]
Когда мы добавляем соль Мп 1 1, мы этим уменьшаем инкубационный период; образующийся промежуточный окисел восстанавливается солью Мп и, таким образом, не может уже проявить своего индуцирующего влияния на окисление соляной кислоты. [9]
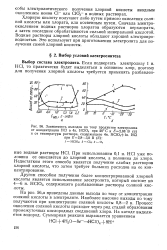 |
Зависимость выходов по току продуктов электролиза от концентрации HCI в 4н. НСЮ4 при 20 С и. 2 88 В ( а и от температуры раствора, содержащего 4н. НСЮ4 1н. НС1. [10] |
На рис. 56 а приведены данные выхода по току от концентрации соляной кислоты в электролите. Процесс окисления соляной кислоты проходит через ряд стадий образования промежуточных кислородных соединений хлора. На катоде выделяется водород. [11]
Если надо определить хлориды в присутствии относительно больших количеств бромидов, рекомендуется производить определение при несколько большей кислотности. Возможное тогда окисление соляной кислоты предупреждается добавлением coin двухвалентного марганца. [12]
Раствор перед титрованием необходимо охладить и разбавить в несколько раз холодной дистиллированной водой. В горячем растворе возможно окисление соляной кислоты марганцовокислым калием. [13]
Раствор перед титрованием необходимо охладить и разбавить несколько раз холодной дистиллированной водой. В горячем растворе возможно окисление соляной кислоты марганцевокислым калием. [14]
Хлор был впервые получен Шееле окислением соляной кислоты двуокисью марганца. Эта реакция лежит в основе метода Велдона, предусматривавшем регенерацию двуокиси марганца. Позже был разработан метод Дикона, основанный на окислении хлористого водорода кислородом воздуха или чистым кислородом. [15]
Страницы: 1 2