Окисление - ксилол
Cтраница 2
Для условий окисления ксилолов коэффициенты массоотдачи жидкой и газовой фаз могут быть приняты PI. При этих значениях PL, о и Я, как показали расчеты, до значения / пп-50 диффузия в газовой фазе практически не влияет на скорость абсорбции кислорода. [16]
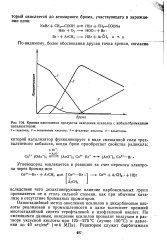 |
Кривые накопления продуктов окисления ксилолов с кобальтбромидным катализатором. [17] |
Одностадийный метод окисления ксилолов в дикарбоновые кислоты реализован в промышленности и даже вытесняет прежний многостадийный синтез терефталевой и изофталевой кислот. [18]
Применительно к окислению ксилолов образующиеся в качестве промежуточных продуктов толуиловые кислоты окисляются труднее чем сами ксилолы. [19]
Найдено, что окисление ксилола с растворенным в нем гидрохиноном или яара-фенилендиамином или без них сильно ускоряется светом в присутствии катализаторов. [20]
Характеристики предельных режимов окисления ксилола, несообщаемые в работе [426], легко вычислить. [21]
Вопрос о механизме окисления ксилолов тоже остается еще далеко не ясным. Варфоломеева выделила гидроперекись п-ксилола и предложила цепную схему реакции. [22]
В качестве катализаторов окисления ксилолов наибольшее распространение получили соли тяжелых металлов ( кобальта, марганца, циркония, церия и др.), бромсодержащие соединения ( бромистоводородная кислота, тетрабромэтан, бромиды переходных и непереходных металлов), которые используют в виде бинарных, тройных и более сложных смешанных каталитических систем. В данном разделе изложены вопросы кинетических закономерностей реакционной способности и механизма жидкофазного окисления изомерных ксилолов, а также приведены принципиальные схемы технологических процеосое получения ароматических дикарбоновых кислот. [23]
Характеристики предельных режимов окисления ксилола, несообщаемые в работе [426], легко вычислить. [24]
Анализ ксилолов производится окислением ксилола водным раствором хамелеона. Навеска ксилола помещается в колбу с обратным холодильником, снабженную мешалкой. Раствор хамелеона подогревается на водяной бане и окисление продолжают до исчезновения розовой окраски хамелеона, взятого в избытке против) теории. В случае присутствия в ксилоле бензина, необходим значительный избыток хамелеона. По окончании окисления, раствор еще горячим отфильтровывается от перекиси марганца, слой углеводородов не окисленных удаляется и раствор полученных кислот упаривается до половины объема. Далее к холодному раствору прибавляют соляной кислоты до кислой реакции, причем выпадают изо - и терефталевая кислоты. Разделение этих кислот достигается в виде бариевых солей, так как соль терефталевой кислоты плохо растворима. Свободные кислоты с этой целью переводятся в аммиачные соли; к раствору этих солей, лучше крепкому, приливают раствор хлористого бария, нагревают и дают остыть. Садится бариевая соль терефталевой кислоты. Для очистки эту соль растворяют в соляной кислоте ( слабой) и переосаждают свободную кислоту снова барием через аммиачную соль. В результате остается изофта левая кислота. Фильтрат, полученный при первом осаждении соляной кислотой смеси изо - и терефталевой кислоты, содержит фталевую и бензойную кислоту, причем последняя растворима в хлороформе. Охлажденный фильтрат трижды извлекают хлороформом и ив вытяжек осторожным испарением выделяют бензойную кислоту. Извлеченный раствор содержит всю фталевую кислоту и небольшое количество изофталевой, которая осаждается первой при упаривании раствора. В качестве примера автор приводит следующий: 35 г фракции 134 - 143, уд. Окисление велось 12 часов, избыток хамелеона устранялся введением. Оставшийся не окисленным слой имел уд. Фильтрат был затем выпарен до 200 см3 и переработан по вышеуказанному способу. [25]
Фталевые кислоты получают окислением соответствующих ксилолов. [26]
Установлено, что при окислении ксилолов в среде уксусной кислоты в присутствии кобальт-марганец - брО1мидного катализатора реакционная способность изомеров к окислению согласуется с результатами, полученными при конкурирующем окислении-в отсутствие растворителя ( см. с. В развившемся процессе окисления о-ксилола торможение реакции наблюдается на стадиях превращения о-карбоксибенз-альдегида. [27]
Большой промышленный интерес представляют процессы окисления ксилолов во фталевый ангидрид и фталевые кислоты ( стр. [28]
Большой промышленный интерес представляют процессы жид-кофазного окисления ксилолов, при которых, в зависимости от условий реакции, получаются различные кислоты 5: толуиловые ( о -, м -, п -), изофталевая и терефталевая. [29]
Большой промышленный интерес представляют процессы жид-кофазного окисления ксилолов, при которых в зависимости от условий реакции получаются различные кислоты: толуиловые ( о -, м -, п -), ортофталевая, изофталевая и терефталевая. [30]
Страницы: 1 2 3 4