Окисление - метан
Cтраница 1
 |
Схема получения формальдегида окислением метана. [1] |
Окисление метана в присутствии платины и палладия в качестве катализаторов до образования муравьиной кислоты и продуктов полного окисления ( СО2 и Н2О) происходит так быстро, что выделить промежуточные продукты окисления ( формальдегид, метанол) не удается. [2]
 |
Схема получения формальдегида окислением метана. [3] |
Окисление метана при атмосферном давлении приводит главным образом к образованию формальдегида. При высоком давлении и большом избытке метана в газовой смеси основным продуктом является метиловый спирт. [4]
Окисление метана наблюдается и при действии воды в присутствии катализатора при высокой температуре. [5]
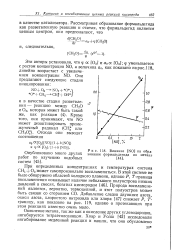 |
Влияние [ NO ] на образование формальдегида из метана. [6] |
Окисление метана, так же как и окисление других углеводородов, ингибируется тетраэтилсвинцом. [7]
Окисление метана кислородом воздуха в формальдегид в присутствии станната и ванадата кальция разработано С. С. Медведевым и представляет большой практический интерес, так как позволяет использовать природные углеводородные газы для получения многих весьма ценных продуктов. [8]
Окисление метана кислородом при атмосферном давлении под действием быстрых электронов с энергией 15 кэв ведет к образованию газообразных продуктов - Нг, СО и СОг и жидких продуктов - перекиси водорода, формальдегида, метилового спирта, муравьиной кислоты и воды. Изменение температуры от - 78 до 150 С мало влияет на скорость окисления, но существенно сказывается на соотношении продуктов реакции между жидкими и газообразными продуктами: от 9: 1 при - 78 С до 1: 2 при 150 С. При уменьшении давления с 760 до 190 мм рт. ст. конверсия метана уменьшается. Изменение концентрации метана в смеси с 50 до 80 % приводит к увеличению скорости окисления и радиационно-химического выхода прореагировавшего метана. При увеличении концентрации метана до 90 % скорость окисления уменьшается, но выход жидких продуктов увеличивается. [9]
Окисление метана может протекать только по высокотемпературному механизму. При атмосферном давлении и температуре ниже 400 С сколько-нибудь значительного окисления не происходит; при температуре до 500 С скорость окисления еще не велика. Важнейшими продуктами реакции являются окись углерода и вода. [10]
Окисление метана окисью цинка было предложено Ооегпег ом 18 в качестве метода для очистки цинка. [11]
Окисление метана до окиси углерода и водорода является перспективным методом получения технологического газа для синтеза аммиака, спиртов и моторного топлива. [12]
Окисление метана в метанол сопровождается включением в молекулу одного атома кислорода; эту реакцию катализирует метаноксигеназа. [13]
Окисление метана воздухом в присутствии катализаторов дает метиловый спирт СН3ОН, формальдегид НСНО, муравьиную кислоту НСООН. [14]
Окисление метана объясняет и появление части воды на планете. Оставшаяся же часть метана была погребена в недрах Земли. [15]
Страницы: 1 2 3 4