Окисление - платина
Cтраница 1
Окисление платины протекает при высоких температурах и повышенной концентрации кислорода и хлорсодержащего реагента ( например, дихлорэтана) в количестве, эквивалентном до 1 0 % хлора от массы катализатора. [1]
Окисление платины до Pt ( IV) при рН 8 при помощи бромат-иона с последующим кипячением приводит к осаждению в виде гидра-тированного окисла всего присутствующего палладия, a Pt ( IV) остается в растворе. В других случаях методы, предложенные для осаждения палладия из растворов, применимы и для платины. Тиосемикарбазид и фенилтиосемикарбазид в слабокислых средах образуют с Pt ( IV) окрашенные комплексы. [2]
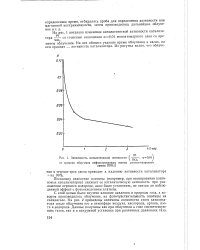 |
Зависимость каталитической активности. [3] |
Поскольку окисление платины ( например, при озонировании платиновых катализаторов) снижает ее каталитическую активность при разложении перекиси водорода, надо было установить, не связан ли наблюденный эффект с фотоокислением платины. [4]
Во избежание окисления платины в раствор следует пропускать углекислый газ. [5]
Тот же необратимый характер процессов окисления платины прослеживается и на потенциодинамических кривых ( рис. 1.6, б), которые широко стали изучаться после появления в арсенале исследователей электронных по-тенциостатов. Последний позволяет задать линейный закон изменения потенциала изучаемого электрода ( по отношению к электроду сравнения); при этом регистрируется ток через границу электрод - раствор. [6]
 |
Свойства сйежих НК. [7] |
Химическими называют потери, вызванные окислением платины кислородом ABC до РЮа. Температура плавления и кипения оксида платины составляет 450 и 477 С соответственно. [8]
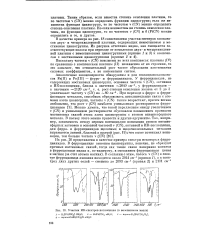 |
Участки ИК-спектров поглощения ( в вазелиновом масле. [9] |
Таким образом, если известна степень окисления платины, то по частотам v ( CN) можно определить функцию цианогрупп; если же неизвестна функция цианогрупп, то по частотам v ( CN) можно определять степень окисления платины. Но если неизвестны ни степень окисления платины, ни функция цианогрупп, то по частотам v ( CN) и б ( PtCN) можно определить и то, и другое. [10]
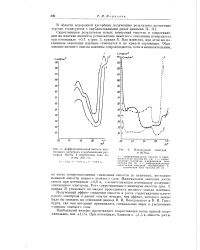 |
Дифференциальная емкость платинового электрода в разбавленных растворах ШЗСи в переменном токе частоты 200 гп. [11] |
Как известно, при этом же потенциале окисление платины отмечается и на кривой заряжения. [12]
В первом случае, очевидно, положительная степень окисления платины равна двум, во втором случае - четырем. [13]
Отсюда делается вывод о том, что анодная реакция заключается в окислении платины; за ней следует химическое окисление перекиси образовавшимся окислом. При катодном импульсе, следующем за анодным, впервые появляется катодная задержка, с увеличением числа парных импульсов последняя растет до определенного предела. [14]
Наиболее распространенный метод отделения платины от сопутствующих платиновых металлов состоит в окислении платины броматом до четырехвалентного состояния и последующем гидролитическом осаждении примесей гидрокарбонатом натрия. После такой обработки в фильтрате, содержащем платину, находятся также растворенные соли натрия. Перед обработкой сероводородом фильтраты, содержащие платину, выпаривают с соляной кислотой, чтобы разрушить бромат. При этом происходит взаимодействие значительного количества хлорида натрия с платиной. [15]
Страницы: 1 2 3 4