Окисление - бромид
Cтраница 2
Метод основан на окислении бромида в бромат гипохлоритом калия и определении бромат-иона катодной поляризацией ( см. стр. Бромиды определяют при содержании от 10 - 3 г / л и более. [16]
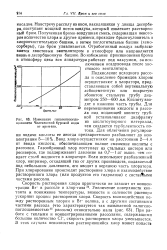 |
Изменение галогенопогло. [17] |
Подкисление исходного рассола и окисление бромидов хлором осуществляют в хлораторе, представляющем собой вертикальную асбоцементную или покрытую эбонитом стальную трубу диаметром 250 - 600 мм. Кислоту вводят в нижнюю часть трубы. Для перемешивания кислоты и рассола над подающей кислоту трубкой устанавливают диафрагму из кислотоупорного материала, чем создается турбулентность потока. Газообразный хлор поступает из стальных цистерн или ресиверов, где поддерживают давление на 0 7 - 1 ат выше, чем создает столб жидкости в хлораторе. Если используют разбавленный хлор, например, отходящий газ от других производств, подаваемый под небольшим давлением, его вводят в верхнюю часть хлоратора. При хлорировании происходит растворение хлора и взаимодействие растворенного хлора ( или продуктов его гидролиза) с составными частями рассола. [18]
 |
Ионный состав воды. [19] |
Для последующею проведения процесса окисления бромида необходимо провести процесс удаления диоксида углерода СО2, т.е. декарбонизации. Этот процесс идет в кислой среде ( РН 2 - 2 5) при продувке умеренно нагретым воздухом, подкисленной соляной кислотой воды. Удаление ( отдувка) СО2 должна быть полной. [20]
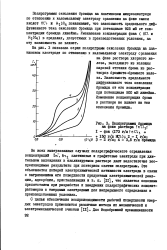 |
Полярограммы бромида на фоне раствора РеиЦ. [21] |
Зависимость предельного диффузионного тока окисления бромида от его концентрации при потенциале 900 мВ линейна. Изменение концентрации брома в растворе не влияет на ток окисления бромида. [22]
В лабораториях бром получают окислением бромидов калия или натрия в кислой среде диоксидом марганца при нагревании. [23]
В лабораториях бром получают окислением бромидов калия или натрия в кислой среде двуокисью марганца при нагревании. [24]
Метод, основанный на окислении бромида до бромата, первоначально разработан ван дер Мейленом [28, 29] и применим в присутствии больших количеств хлорида. [25]
Бром, полученный при окислении бромида броматом в растворе серной кислоты, взаимодействует с красителями типа фенолового красного с образованием сильно окрашенных соединений, светопоглсщение которых измеряют фотометрически. Определение брома с крезоло-вым красным ( о-крезолсульфофталеин), взаимодействующего с двумя атомами брома, гораздо чувствительнее широко известного метода с применением фенолового красного [13], который реагирует с четырьмя атомами брома. Исследуемый раствор не должен содержать соляной или азотной кислоты, так как они разрушают краситель. [26]
Целый ряд окислителей используется для окисления бромида до свободного брома, который отгоняется или экстрагируется, а затем определяется иодометрически. Надлежащий подбор окислителя позволяет проводить избирательное окисление бромида в присутствии хлорида. Окислителями могут служить пер-манганат в сочетании с соляной или фосфорной кислотой или сульфатом меди, а также хромовая кислота в сочетании с серной или азотной кислотой. При использовании последнего сочетания и экстракции брома 53 иодид превращается в иодат и не оказывает мешающего влияния. При содержании хлорида натрия более 75 мг в 100 мл результаты определения оказываются повышенными. [27]
Сабо и Чаньи 56 изучали окисление бромида свободным хлором и установили, что оно протекает в две стадии. При рН 6 5 - 7 5 образуется бромноватистая кислота НОВг, которая подвергается гидролизу с образованием бромата. При рН 8 5 - 9 гидролиз идет достаточно быстро, что делает реакцию вполне пригодной для аналитических целей. [28]
В зависимость предельного диффузионного тока окисления бромида от его концентрации линейна. Это позволяет применить полярографический метод для прямого определения концентрации бромида в поступавших и сбросных водах бромных производств. [29]
 |
Аналитические характеристики индика / порны - реакций. [30] |
Страницы: 1 2 3 4