Окисление - ртуть
Cтраница 2
Электрохимическое поведение, кинетика окисления ртути ( I) и восстановления ртути ( II) хорошо изучены. Установлены оптимальные значения Ер. [16]
Химическая обработка основана на окислении ртути с превращением ее в оксид или хлорид. Метод, основанный на взаимодействии ртути с 20 % - ным водным раствором хлорида железа, считается одним из наиболее простых и надежных. Обрабатываемую поверхность обильно смачивают раствором и несколько раз протирают щеткой для лучшего эмульгирования ртути, а затем оставляют до полного высыхания. [17]
 |
Схема обогрева парами ртути. [18] |
Для того чтобы не происходило окисления ртути, ртутный трубопровод соединяют с сосудом 5, в котором поддерживается давление азота. [19]
На рис. 3.15 показаны полярограммы окисления ртути в присутствии сульфида. [20]
 |
Схема простейшей поляро-графической установки. [21] |
При анодной поляризации РКЭ возникает ток окисления ртути при потенциале 0 35 В. Так как подаваемое напряжение практически полностью приходится на РКЭ, то ионы Zn2 быстро разряжаются у поверхности электрода и концентрация их становится равной нулю. Подача новых ионов к электроду в присутствии фонового электролита и в отсутствие перемешивания осуществляется лишь за счет диффузии, скорость которой пропорциональна концентрации ионов Zn2 в растворе. Наступает предельное состояние, при котором дальнейшее увеличение отрицательного напряжения не вызывает увеличения тока в цепи. Диффузионным ( предельным) током называют такой ток, который протекает в полярографической ячейке при добавлении определяемых ионов к поверхности ртутной капли только за счет диффузии и который пропорционален концентрации определяемого вещества в растворе. [22]
В результате этого полностью исключается возможность окисления ртути, связанная с нестопроцентным выходом по току в электролизере. [23]
В растворах цианидов волна таллия маскируется волной окисления ртути. [24]
Различные методы химической обработки основаны либо на окислении ртути с превращением ее в оксид или в хлорид, либо на переведении ее в мелкодисперсное состояние, что облегчает уборку. Однако следует иметь в виду, что ртуть в химическом отношении весьма устойчива. По этой причине химические дегазирующие агенты способны окислить только поверхность ртути и, следовательно, эффективны при обработке лишь очень мелких капель. На более крупных каплях образуется защитная пленка, однако эффект снижения концентрации паров ртути в воздухе оказывается лишь временным. При повышении температуры или механическом воздействии оксидная пленка растрескивается и испарение ртути возобновляется. [25]
Этими опытами впервые было установлено, что процесс окисления ртути состоит в соединении ее со здоровой частью воздуха. Результаты своих опытов он изложил в докладе Академии наук 26 апреля 1775 г., а 8 августа 1775 г. он еще раз повторил доклад, в котором впервые разъяснил, что воздух состоит из двух газов: чистого воздуха, способного поддерживать горение, дыхание и окислять металлы, и воздуха, не обладающего этими свойствами. [26]
Конечную точку определяют также по появлению анодного тока окисления ртути в присутствии избытка комплексона III. Раздельное определение основано на разной устойчивости комплексонатов определяемых элементов в соответствующей среде. [27]
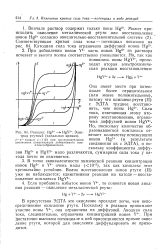 |
Реакция. Hg2 - - HgY2 -. Электрод ртутный ( идеальная кривая. [28] |
В присутствии ЭДТА это окисление проходит легче, чем непо-средственное окисление ртути. Поскольку в реакции принимают участие ионы Y4 -, она ограничена их диффузией. При достаточно высоком потенциале к ней присоединяется прямое окис ление ртути, которой для окисления диффундировать не прихо дится. [29]
При отсутствии в ртути щелочного металла под дей-твием окислителей происходит окисление ртути, и на раздела, в силу большого поверхностного на - яжения, ртуть стремится к естественному краевому углу; смачивание прекращается и ртуть постепенно собирается в отдельные лужицы и капли. Для длительного сохранения амальгамы железа при отсутствии в ртути щелочного металла нужно защищать амальгамированную поверхность от доступа окислителей, например, погружением под слой ртути толщиной более 3 мм или в освобожденный от кислорода раствор. [30]
Страницы: 1 2 3 4