Окисление - сульфид
Cтраница 2
Окисление сульфидов до тиосульфатов идет при химической их реакции с растворенным в воде кислородом. [16]
Окисление сульфидов в сульфоны, проходящее под действием гидроперекисей в присутствии оснований, обстоятельно исследованное в ряде работ [374, 375], не относится к предмету нашего обсуждения. [17]
Окисление сульфидов перманганатом калия чаще всего проводят в растворе уксусной или серной кислоты. [18]
Окисление сульфидов перекисью водорода в спиртовой среде, подавляющей диссоциацию, сопровождается образованием сульфатов железа. Когда окисляется моносульфид железа ( FeS), то при сохранении соотношения железа и серы 1: 1 может образоваться только Fe ( OH) SO4 [ 2FeS 9H2O2 2Fe ( OH) SO4 8H2O ], основная соль, покрывающая поверхность зерен моносульфида пленкой, защищающей их от дальнейшего окисления. Это - соль, растворимая в водно-спиртовой среде и не мешающая дальнейшему окислению дисульфида железа. [19]
Окисление сульфидов в сульфоксиды и сульфоны. [20]
 |
Окислительная печь Клауса для регенерации серы. [21] |
Окисление сульфидов, основанное нац указанных выше реакциях, называют процессом Клауса и проводится в печах окислительных Клауса в присутствии катализатора боксита. [22]
Окисление сульфидов ( лучше всего перекисью водорода в уксусной кислоте) дает сульфоксиды и сульфоны. Степень окисления определяется соотношением реагентов, и могут быть получены с хорошими выходами как сульфоксид, так и сульфон. [23]
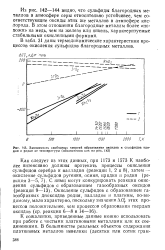 |
Зависимость свободных энергий образования оксидов и сульфидов иридия и родия от температуры ( обозначения как на 142. [24] |
Окисление сульфидов с образованием газообразных диоксидов родия, палладия и платины, по-видимому, мало характерно, поскольку значения Д6 этих процессов положнтельнее, чем процессов образования твердых оксидов ( ср. [25]
Окисление сульфидов протекает в две стадии. [26]
Окисление сульфидов гексацианоферратом ( III) приводит к образованию различных продуктов реакции в зависимости от условий ее протекания. Конечную точку находят потенциометрически или по исчезновению красной окраски комплекса железа ( II) с диметилглиоксимом. [27]
Вышеописанное окисление сульфидов в сульфоксиды может проводиться также и с использованием ацетонированной культуры A. Получение ацетонированной культуры представляет собой первую стадию одного из обычных методов выделения и очистки фермента. [28]
Окисление сульфидов гексацианоферратом ( III) приводит к образованию различных продуктов реакции в зависимости от условий ее протекания. Конечную точку находят потенциометрически или по исчезновению красной окраски комплекса железа ( II) с диметилглиоксимом. [29]
Окисление сульфидов гексацианоферратом ( III) приводит к образованию различных продуктов реакции в зависимости от условий ее протекания. [30]
Страницы: 1 2 3 4