Окисление - насыщенные углеводород
Cтраница 3
Следовательно, соединения бора не являются катализаторами окисления, они лишь повышают селективность при окислении насыщенных углеводородов ( увеличение выхода спиртов) и олефинов ( увеличение выхода эпоксидов), способствуя нерадикальному окислению углеводородов промежуточно образующимся гидропероксидом. Ал-килароматические углеводороды не могут быть окислены в присутствии соединений бора. [31]
Схемы механизма образования кислородсодержащих соединений ( гидропероксидов, спиртов, карбонильных соединений, кислот, лактонов) при окислении насыщенных углеводородов рассмотрены выше. [32]
Необходимо отметить, однако, что до сего времени ни разу не было строго доказано, что гидроперекись является единственным первичным продуктом при окислении насыщенных углеводородов нормального строения, протекающего с достаточными скоростями при 130 - 160 С. [33]
Несмотря на это, схема Льюиса и Эльбе, обладающая кажущейся логической стройностью, пожалуй, в большей степени, чем другие цепные схемы окисления насыщенных углеводородов, формальна, что обусловлено недостаточным экспериментальным обоснованием и вытекающей отсюда гипотетичностью отдельных участвующих в ней элементарных превращений. [34]
К теории Виланда близко примыкают взгляды Льюиса [71], который, критикуя перекисную теорию и факты, приводимые в пользу ее Каллендером, считает, что первичной реакцией окисления насыщенных углеводородов является отщепление водорода под действием молекулярного кислорода с появлением воды и ненасыщенного остатка, из которого далее могут образоваться перекиси и альдегиды. [35]
Поскольку трифторуксусная кислота в комбинации с подходящими электролитами обладает широким анодным окном ( до 2 1 В относительно Ag / Ag и 2 3 В относительно нас.к.э.) [210, 213], в этой системе становится возможным окисление насыщенных углеводородов. Запись кривых плотность тока - потенциал в стационарном состоянии и препаративный ЭКП этих субстратов часто выполняют при импульсной активации электрода. Этот процесс включает короткую периодическую пульсацию потенциала электрода до величины примерно О В, что предотвращает чрезмерное падение тока при рабочем потенциале. На основании электрохимических измерений предполагается, что до лимитирующей стадии и в ней самой происходит перенос одного электрона. [36]
Широко исследовано применение для окисления алканов окислителей на основе переходных металлов. Окисление насыщенных углеводородов неорганическими окислителями идет в довольно жестких условиях; поскольку первоначальные продукты реакции обычно более склонны к окислению, чем сами алканы, образуются значительные количества продуктов вторичного окисления. Трудно, например, окислить метиленовую группу во вторичную спиртовую группу без дальнейшего окисления в кетонную группировку; в некоторых случаях условия окисления настолько жесткие, что происходит расщепление С-С - связи. Обычно удается превратить С - Н - группы в третичные спиртовые группы, однако поскольку многие третичные спирты легко дегидратируются, то, их, как правило, нельзя получить с хорошим выходом. Низшие алканы ( d - 4) окисляются до спиртов кислородом в ацетонитриле при комнатной температуре в присутствии хлорида олова ( II); при этом метан значительно менее реакционноспособен, чем этан, пропан и бутан. Использование солей Со ( III) для каталитического окисления бутана в уксусную кислоту представляет промышленный интерес. Окисление н-пентана также дает уксусную кислоту в качестве главного продукта; в состав минорных продуктов входят пропановая, бутановая и пентановая кислоты. [37]
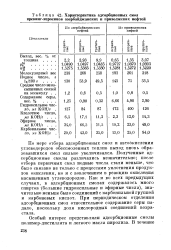 |
Характеристика адсорбционных смол крекинг-керосинов азербайджанских и приволжских нефтей. [38] |
По мере отбора адсорбционных смол и автоокисления углеводородов обессмоленных топлив выход вновь образовавшихся смол сильно увеличивался. Полученные адсорбционные смолы различались незначительно; после отбора первичных смол йодные числа стали меньше, что было связано не только с процессами уплотнения продуктов окисления, но и с вовлечением в реакцию окисления насыщенных углеводородов. Как и во всех предыдущих случаях, в адсорбционных смолах содержалось много спиртов - ( большие гидроксильные и эфирные числа), значительно меньше было соединений с карбонильной группой и карбоновых кислот. [39]
Например, для 95 6 % - ной кислоты имеем k 0 008 ч - 1, причем энергия активации составляет 21 - 29 кДж / моль. Однако наибольшую скорость реакции наблюдали в присутствии 99 8 % - ной кислоты, что связывают с возрастанием роли побочных реакций для более сильных растворов. Действительно, концентрированные растворы HaS04 участвуют в реакциях сульфирования и окисления насыщенных углеводородов. [40]
Окисление начинается лишь в жестких условиях, например под действием горячей хромовой смеси. При этом получаются кетоны, кислоты и другие продукты окисления. Поэтому окисление насыщенных углеводородов не является препаративным методом получения определенных соединений. [41]
Окисление начинается лишь в жестких условиях, например под действием горячей хромовой смеси. При этом получаются кетоны, кислоты и другие продукты окисления. Поэтому окисление насыщенных углеводородов не является препаративным методом получения определенных соединений. [42]
Окисление начинается лишь в жестких условиях, например под действием горячей хромовой смеси. При этом получаются кетоны, кислоты п другие продукты окисления. Поэтому окисление насыщенных углеводородов не является препаративным методом получения определенных соединений. [43]
Окисление начинается лишь в жестких условиях, например под действием горячей хромовой смеси. При этом получаются кетоны, кислоты и другие продукты окисления. Поэтому окисление насыщенных углеводородов не является препаративным методом получения определенных соединений. [44]
Превращение метана и его более высокомолекулярных гомологов в формальдегид путем прямого окисления с помощью металлических или окисно-металлических катализаторов было бы экономически выгодным методом, если бы выходы формальдегида были достаточно высокими. В одной из заявок [50] предлагается метод получения формальдегида с достаточно высокими выходами при окислении метана над нанесенными металлическими катализаторами. Из полученных результатов следует, что процесс, определяющий скорость реакции, зависит в первую очередь от структуры углеводорода. Этот механизм укладывается в представление Волькенштейна [28], который предположил, что слабую хемосорб-цию можно рассматривать как совместное владение квазисвободными электронами - адсорбатом и адсорбентом ( см. разд. Таким образом, предложенная Любарским схема окисления насыщенных углеводородов связана с взаимодействием хемосорбированных углеводородных радикалов либо с газообразным, либо с хемосорбированным кислородом. [45]
Страницы: 1 2 3