Окисление - хлорат
Cтраница 2
Как указывалось ранее, при любом из перечисленных выше механизмов окисления хлората до перхлората получению высоких выходов по току должна способствовать высокая концентрация хлората в электролите. По мере уменьшения концентрации хлората в электролите выход по току должен снижаться, особенно после достижения предельной критической концентрации хлората. При введении добавок фторидов выхода по току на анодах из РЬО 2 значительно возрастают. В табл. 8 - 8 приведены данные о зависимости выхода по току от концентрации хлората на различных анодах. [16]
На графитовых анодах не достигается потенциал, необходимый для протекания реакции (7.13), поэтому окисления хлората до перхлората практически не наблюдается. [17]
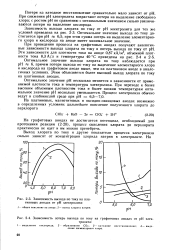 |
Зависимость выхода по току на платиновых анодах от рН электролита.| Зависимость потерь выхода по току на графитовых анодах от рН электролита. [18] |
На графитовых анодах не достигается потенциал, необходимый для протекания реакции ( 2 - 20), процесс окисления хлората до перхлората практически не идет и им можно пренебречь. [19]
На графитовых анодах могут протекать процессы окисления водных растворов хлоридов щелочных металлов до элементарного хлора, гипохлоритов и хлоратов, однако невозможно осуществить окисление хлоратов до перхлоратов. На платиновых анодах с высоким перенапряжением выделения кислорода электрохимический синтез перхлоратов протекает с хорошим выходом по току, по на платиновых анодах невозможно достичь высокой степени окисления хлорида до хлората без параллельно протекающего при этом процесса синтеза перхлората в той или иной степени. При проведении на аноде электрохимического синтеза органических соединений в качестве анода необходимо также применять материалы с высоким перенапряжением для выделения кислорода. [20]
Выделение кислорода протекает с малой скоростью на платиновых анодах, которые достаточно устойчивы даже при высоком положительном потенциале, необходимом для проведения реакции окисления хлората в перхлорат. В связи с этим в производстве перхлоратов, как правило, используются платиновые аноды. В последние годы изучаются аноды из двуокиси свинца, которые призваны заменить платину. [21]
Повышается не только вследствие того, что предотвращается восстановление хлората на катоде, но и, по мнению авторов [124], благодаря тому, что бихромат препятствует окислению хлората в перхлорат на аноде, которое возможно при низких концентрациях хлорида. [22]
Перспективным является непосредственное получение хлорной кислоты электролизом соляной кислоты, известное еще с конца прошлого века. При этом на аноде протекает одновременно окисление растворенного хлора, образование хлорноватой кислоты и окисление хлората в перхлорат; на катоде происходит выделение водорода. [23]
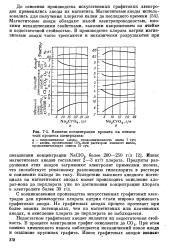 |
Влияние концентрации хромата на показатели процесса электролиза. [24] |
С возникновением производства искусственных графитовых электродов для производства хлората натрия стали широко применять графитовые аноды. На графитовых анодах процесс протекает при более низких потенциалах, чем на магнетитовых или платиновых анодах, и окисление хлората до перхлората не наблюдается. [25]
Обычно считают, что образование перхлората протекает в две стадии: 1) окисление хлорида до хлората; 2) окисление хлората до перхлората. В первой стадии целесообразно применять графитовые или магнетитовые аноды, либо аноды из двуокиси свинца. Во второй стадии рекомендуются платиновые аноды, а также аноды из двуокиси свинца. В отличие от этой схемы авторы предлагают получать перхлорат натрия в одну стадию непосредственно путем электролиза хлористого натрия. [26]
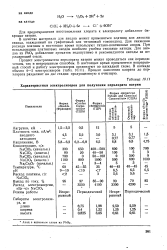 |
Характеристики электролизеров для получения перхлората натрия. [27] |
Процесс электросинтеза перхлората натрия может проводиться как периодическим, так и непрерывным способом. В настоящее время применяется непрерывный способ и работу электролизеров организуют по каскадной схеме. Процесс окисления хлората до перхлората разделяют на две стадии: продукционную и очистную. [28]
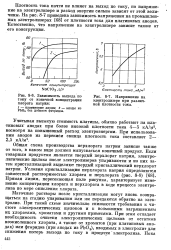 |
Зависимость выхода по току от конечной концентрации хлората натрия. 1 - платиновые аноды. 2 - аноды из PbOj без добавок фторидов.| Напряжение на электролизере при различной плотности тока. [29] |
Общая схема производства перхлората натрия зависит также от того, в каком виде должен выпускаться конечный продукт. Если товарным продуктом является твердый перхлорат натрия, электролитические щелока после электролизеров упариваются и из них затем кристаллизацией выделяют твердый кристаллический перхлорат натрия. Прямая линия, пересекающая поле рисунка, характеризует изменение концентрации хлората и перхлората в ходе процесса электролиза по мере окисления хлората. [30]
Страницы: 1 2 3