Окисление - холестерин
Cтраница 1
Окисление холестерина, вызванное действием излучения. [1]
Окисление холестерина тет ] аацетатом свинца протекает очень медленно даже при 60; при этом не удалось выделить индивидуального продукта реакции. Эргостерин легко вступает в реакцию с тем же реагентом и присоединяет две гидроксильные или ацетоксильные группы к двойной связи в положении 5 6, образуя 3 6-диацетат триола VIII614 с 15 - 20 % - ным выходом. [2]
Теоретически окисление холестерина может дать 4 моля уксусной кделоты. [3]
При окислении холестерина гипобромитом в щелочном растворе 5 - образуется ненасыщенный продукт, так называемая кислота Дильса. Карбоксильная группа при кольце В испытывает пространственные затруднения, и при этерификации по Фишеру кислота образует только моноэфир. [4]
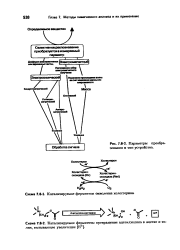 |
Параметры преобра. [5] |
Катализируемое ферментом окисление холестерина. [6]
Синтетически тестостерон получают окислением холестерина хромовым ангидридом. Чтобы при окислении не разрушилось стероидное ядро, холестерин перед окислением ацетилируют, а двойную связь защищают путем присоединения брома. [7]
Синтетически тестостерон получают окислением холестерина хромовым ангидридом. Чтобы при окислении не разрушилось стероидное ядро, холестерин перед окислением ацетнлируют, а двойную связь защищают путем присоединения брома. [8]
Эта реакция широко применяется для окисления холестерина и других гомоаллиловых Д5 - стенолов. [9]
Розенгейм и Стерлинг [18] осуществили окисление холестерина ( 10) в ДГ ] - холестенднол - Зр 4р ( 11); при этом атаке подвергается а-положение к наиболее замещенному непредельному атому углерода. Дальнейшая обработка состоит в прибавлении 100 г ацетата натрия и быстром нагревании смеси для превращения коллоидального селена в черный селен. [10]
Интересным вариантом этой реакции является окисление холестерина XLI щелочным раствором гипобромита [41] в ненасыщенную кислоту Дильса XLII ( фрагмент молекулы) с раскрытием кольца А. Вероятный механизм этой реакции состоит в первичном окислении спирта в кетон с последующим образованием карб-аниона, бромированием, расщеплением кольца и окислением. [11]
Продукты, образующиеся в результате окисления холестерина по Оппенауеру и вследствие отнятия галоидоводорода от солянокислого холестена, называются соответственно холестеноном и Д4 - холестеном, а не копростеноном и копростеном, как это было предложено Розенхеймом и Кингом. Обе окиси холестерина адэкватно описываются их тривиальными названиями, поэтому мы предпочитаем название Р - ОКИСЬ холестерина названию 5 ( 3 6р - оксидокопростан-3 [ 3-ол. [12]
Выделение оксилактона IV из продуктов окисления холестерина указывает на образование третичного спирта в качестве промежуточного продукта. [13]
Прегненолон является также одним из продуктов окисления холестерина ( стр. Эти синтезы имеют очень большое значение, так как прогестерон в настоящее время является важнейшим промежуточным продуктом в одном из синтезов кортизона ( стр. Путем ферментации с некоторыми штаммами Rhizopus в прогестерон можно с хорошим выходом ввести оксигруппу в положение Па. Получающийся таким способом lla - оксипрогестерон является исходным веществом в семистадийном синтезе кортизона. [14]
Прегненолон является также одним из продуктов окисления холестерина ( стр. Эти синтезы имеют очень большое значение, так как прогестерон в настоящее время является важнейшим промежуточным продуктом в одном из синтезов кортизона ( стр. Путем ферментации с некоторыми штаммами Rhizopus в прогестерон можно с хорошим выходом ввести оксигрупну в положение Па. Получающийся таким способом 1la - окснпрогестерои является исходным веществом в семистадппном си тезе кортизона. [15]
Страницы: 1 2 3