Окисление - цинк
Cтраница 4
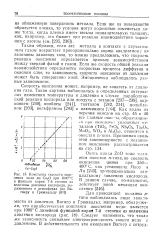
Как показали Верной, Акеройд и Страуд [178], скорость окисления цинка при нагревании до температур ниже 225 С зависит от того, была ли поверхность образца подвергнута шлифовке, травлению или электрохимической полировке. Из рис. 74 видно, что после травления и электрохимического полирования образцы окислялись за одинаковое время быстрее, чем после шлифовки. [46]
Окись цинка ( flores zincl) получается при сожигании или окислении цинка, также при прокаливании разных его солей, напр. Окись, полученная из цинковой обманки ZnS обжиганием ( накаливанием на воздухе, причем сера сгорает в SO2), содержит разнообразные подмеси. Для отделения их полученную окись смешивают с водою и пропускают сернистый газ, образующийся при обжигании обманки. Если раствор этой соли выпарить и полученный остаток прокалить, то остается окись цинка, лишенная многих подмесей. [47]
При наплавке латуни Л62 на сталь с флюсом БМ-1 испарения и окисления цинка не происходит, поэтому получается плотный наплавленный металл, по составу не отличающийся от присадочного металла. [48]
При наплавке латуни Л62 на сталь с флюсом БМ-1 испарения и окисления цинка не происходит, поэтому получается плотный наплавленный металл, по составу не отличающийся от присадочного металла. Наплавка допускается как однослойная, так и многослойная. [49]
Процессы окисления и восстановления в этом случае пространственно не разделены - окисление цинка и образование водорода происходят на поверхности цинка. [50]
 |
Константа скорости окисления меди до Си2О при 1000 С в функции корня 7 - й степени из величины давления кислорода, выраженного в атмосферах ( по Вагнеру и Грюнвальду. [51] |
Окись цинха ZnO тоже является окислом - типа, но скорость окисления цинка при 350 - 400 С, как установили Моор и Ли [245], пропорциональна парциальному давлению кислорода. [52]
Первое число выражает, очевидно, количество теплоты, выделившейся при окислении цинка и количество теплоты, выделившейся при растворении окиси цинка. Вторая величина состоит, естественно, из теплоты, выделившейся при растворении металла, плюс некоторая неизвестная величина. Эту величину мы нашли равной 4371, что почти равно теплоте, выделяемой при окислении водорода. Но очевидно, что при образовании сернокислого цинка растворением цинка, металл окисляется не свободным кислородом, а кислородом, который при взаимодействии с водородом выделил некоторую часть своего тепла. Таким образом, чтобы получить сумму тепла, нужно прибавить всю теплоту, выделяемую при образовании воды, и не принимать в расчет водород. Так как это осуществляется само собой, нам остается только произвести указанное сложение. [53]
Однако в элементе Даниэля - Якоби эта реакция идет так, что окисление цинка Пространственно отделено от восстановления меди. Расчленим происходящую реакцию на отдельные стадии. [54]
Страницы: 1 2 3 4