Окисление - электрод
Cтраница 2
Существенное влияние на профиль пленки электролита оказывает состояние поверхности электрода, которое может изменяться при электрохимическом восстановлении или окислении электрода. В таблице [44] представлены величины толщин пленок, высот менисков и краевых углов в зависимости от состава раствора и предварительной обработки платинового электрода. [17]
Существует мнение [27] о том, что определение свойств диэлектриков при высоких температурах целесообразно проводить в глубоком вакууме, где затруднено окисление электродов и подводящих проводов, а также уменьшается вероятность загрязнения контактов в результате диффузии посторонних примесей из окружающей среды. [18]
В растворе HpSo при 0 5 A / cir на электродах состава М) р т / 2 72 W02 90 Увеличением степени окисления электрода выход по току увеличивается от Т % на W02 I0 до 14 на Wo2 9Q, выход по току озона 0 2J & на окисление электрода идет 0 54 тока. [19]
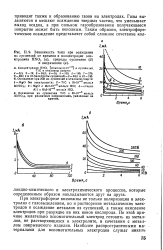 |
Зависимость тока при осаждении из суспензий от времени и концентрации электролита HNO3 ( а, природы суспензии ( б и напряжения ( в. [20] |
При электрофорезе возможны не только поляризация и электролиз с газовыделением, но и растворение металлических электродов и осаждение металлов из суспензий, а также окисление электродов при разрядке на них ионов кислорода. По этой причине желательно вспомогательный электрод готовить из металлов, не растворяющихся в электролите, в сочетании с металлом покрываемого изделия. [21]
Зависимость токов обмена хлорной реакции от концентрации Кц в сплаве аналогична опубликованной в / 1 2 /, Ее сравнение с зависимостью для токов окисления электродов, а также сопоставление стационарных поляризационных кривых, полученных в растворах различных по составу и рН, позволяют предосложить что за разряд С1 - - иона ответственна, в основном, рутениевая компонента, а за окисление электрода ж разряд воды - в основном, титановая компонента окисленной электродной поверхности, причем эта процессы являются конкурентными. [22]
В растворе H So при 0 5 А / см на электродах состава WOo T / J 2 72 2 90 с величвнием степени окисления электрода выход по току увеличивается от 1 % на W02 XJ до 14 на Wo0 9Q, выход по току озона 0 2 на окисление элект зда иде. [23]
В растворе Е О при 0 5 А / см на электродах состава М) р тл 2 72 2 go c Увеличением степени окисления электрода выход по току увеличивается от 7 % на W02 JQ до 14 на Wo2 9Q, выход по току озона 0 2 на окисление электрода идет 0 54 тока. [24]
Ее сравнение с зависимостью для токов окисления электродов, а также сопоставление стационарных поляризационных кривых, полученных в растворах различных по составу и рН, позволяют предположить что за разряд С1 - - иона ответственна, в основном, рутениевая компонента, а за окисление электрода и разряд воды - в основном, титановая компонента окисленной электродной поверхности, причем эти процессы являются конкурентными. Тогда в зависимости от условий, реализующихся на поверхности, можно ожидать преобладания одного зз конкурирующих процессов и, следовательно, либо преимущественного образования CIg, либо хлоркислородных соединений, как следствия взаимодейст-рия дродуктов разряда С1 - - иона и воды. [25]
Ее сравнение с зависимостью для токов окисления электродов, а также сопоставление стационарных поляризационных кривых, полученных в растворах различных по составу и рН, позволяют предположить что за разряд СГ - - иона ответственна, в основном, рутениевая компонента, а за окисление электрода к разряд вода - в основном, титановая компонента окисленной электродной поверхности, причем эти процессы являются конкурентными. [26]
Ее сравнение с зависимостью для токов окисления электродов, а также сопоставление стационарных поляризационных кривых, полученных в растворах различных по составу и рН, позволяют предположить что за разряд С1 - - иона ответственна, в основном, рутениевая компонента, а за окисление электрода и разряд воды - в основном, титановая компонента окисленной электродной поверхности, причем эти процесса. [27]
Ее сравнение с зависимостью дал токов окисления электродов, а также сопоставление стационарных поляризационных кривых, полученных в растворах различных по составу и рН, позволяют предположить что за разряд С1 - - иона ответственна, в основном, рутениевая компонента, а за окисление электрода и разряд воды - в основном, титановая компонента окисленной электродной поверхности, причем эти процессы являются конкурентными. [28]
В растворе Е О при 0 5 А / см на электродах состава М) р тл 2 72 2 go c Увеличением степени окисления электрода выход по току увеличивается от 7 % на W02 JQ до 14 на Wo2 9Q, выход по току озона 0 2 на окисление электрода идет 0 54 тока. [29]
В растворе HpSo при 0 5 A / cir на электродах состава М) р т / 2 72 W02 90 Увеличением степени окисления электрода выход по току увеличивается от Т % на W02 I0 до 14 на Wo2 9Q, выход по току озона 0 2J & на окисление электрода идет 0 54 тока. [30]
Страницы: 1 2 3 4