Окисление - графит
Cтраница 1
Окисление графита при использовании инертных газов может происходить за счет примеси кислорода или вследствие подсоса воздуха, попадающего в газовый тракт. В случае применения углекислого газа радиолитическое восстановление до окиси углерода может привести к значительному уносу графита. Попадание паров воды в кладку в водо-охлаждаемых реакторах создает опасность окисления, так как в результате радиолиза воды образуется кислород. Однако такой способ защиты кроме сложности обладает еще одним недостатком - происходит нежелательное увеличение поглощения нейтронов. [1]
Окисление графита устраняется слабым протоком азота. Распределение температур в стенке печи, дающее представление о работе слоев огнеупорной кладки, количестве аккумулированного тепла и тепловом потоке через стенку, определяется при помощи термопар, закладываемых на определенных расстояниях по толщине стенки. Работа охлаждаемых водой элементов оценивается по показаниям термопар, зачеканенных в их поверхность. [2]
 |
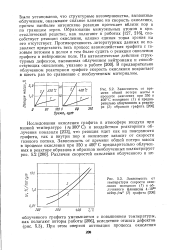
Зависимость износа анодов от кислотности анолита. [3] |
Окисление графита с образованием двуокиси углерода и небольших количеств окиси углерода приводит также к нарушению связи между отдельными зернами графита и механическому осыпанию частиц анода. [4]
Окисление графита ГМЗ сопровождается также некоторым увеличением удельной поверхности. Однако ее величина даже при потере массы 20 % не превышает 2 м2 / г ( 5УД для исходных образцов находится на уровне 1 м2 / г), что указывает на отсутствие микропор как в исходных, так и в окисленных образцах. Рост удельной поверхности пропорционален росту объема пор и увеличению объема определяемых пор. [6]
Продукты окисления графита представляют собой продукты, состав и свойства которых изменяются в зависимости от способов приготовления и обработки. Практически они содержат наряду с углеродом и кислородом некоторое количество водорода. По-видимому, нет никаких данных, говорящих о клатратном связывании кислорода, но имеются доказательства связывания кислорода или водорода в виде простых эфирных, гидроксильных, карбонильных и карбоксильных групп. [7]
Степень окисления графита зависит не только от силы и количества окислителя или от продолжительности электролиза, но и от концентрации и природы внедряющейся кислоты. Так, при избытке окислителя 100 % H2SO4 дает богатую кислотой первую стадию сульфата графита; H2SO4 с концентрацией в 83 % дает лишь вторую стадию бисульфата графита; 63 % H2SO4 дает только третью стадию, а при концентрации менее 50 % бисульфат вообще не образуется. [8]
Температура окисления графита на воздухе составляет - 400 С, а в атмосфере водяного пара и СО2 - соответственно - 700 и 900 С. [9]
Температура окисления графита колеблется в пределах 600 - 700 С в зависимости от природы графита и степени его дисперсности. [10]
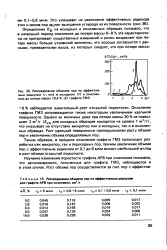
Исследования окисления графита в атмосфере воздуха при низкой температуре ( да 300 С) и воздействии реакторного облучения показали [233], что реакция идет как на поверхности графита, так и внутри пор и окисление зависит от скорости газового потока. [12]
При окислении графита ( в других условиях) азотной кислотой и щелочным перманганатом образуется меллитовая кислота Cj. [13]
При окислении графита смесью H2SO4 и КМпО4 образуется [32] продукт сложного состава. [14]
Кобальт катализирует окисление графита почти так же, как и железо, но остается неясным, почему никель оказывает влияние в течение более продолжительного времени. Одно из возможных объяснений состоит в том, что Ni проявляет катализирующее действие при заметно более низких температурах ( 650 вместо 720 для Fe и Со), образование окисла металла на Ni не может происходить столь легко. [15]
Страницы: 1 2 3 4