Ферментативное окисление
Cтраница 1
Ферментативное окисление а-аминокислот дает 2-оксокисло-ты ( разд. [1]
Полное ферментативное окисление тионовыми бактериями молекулярной серы и различных ее восстановленных соединений приводит к образованию сульфата. [2]
Ферментативное окисление катехинов наблюдается уже при завяливании чайного листа, но наибольшие потери катехинов в результате их окисления происходят во время скручивания и ферментации листа. В связи с этим черный чай, полученный по обычной технологии, содержит всего лишь 10 - 12 % водорастворимых фенольных веществ. [3]
Ферментативное окисление углеводородов нефти происходит в сложной системе, состоящей из нескольких фаз. В водной среде находится в диспергированном состоянии углеводород, там же присутствуют клетки микроорганизмов, находящиеся в коллоидном или близком к коллоидному состоянию. Все это говорит о том, что указанная система является весьма сложной. На чисто химические процессы здесь накладывается влияние факторов, связанных с жизнедеятельностью микроорганизмов, а также с коллоидно-химической природой системы. С этой точки зрения целесообразно рассмотреть механизм проникновения углеводородов в клетку, так как без контакта этих двух составных частей системы невозможно протекание процесса. [4]
Ферментативное окисление боковых цепей белка ( в противоположность окислению проететических групп) является спорным. В ряде статей Сайзер [60, 61] утверждал, что разнообразные белки, в состав которых входит тирозин, - могут быть окислены тирозинаэой либо непосредственно, либо после предварительной обработки их кристаллическим трипсином. [5]
На ферментативное окисление Зр-оксигрунп могут оказывать влияние-даже весьма удаленные заместители. [6]
При ферментативном окислении происходит в небольшом количестве выделение двуокиси углерода, по-видимому, за счет полного окисления части моносахаридов до двуокиси углерода и воды в результате биохимических реакций неустановленного характера, протекающих в живой клетке. [7]
При ферментативном окислении оксиантраниловой кислоты расходуется дин моль кислорода на моль субстрата. [8]
При ферментативном окислении лимонной кислоты поверхность фермента, взаимодействующего с субстратом, создает хиральное окружение субстрата и уничтожает элементы симметрии, бывшие в свободной молекуле субстрата. Комплекс субстрат-фермеит становится диастереотопным. При этом активный центр, обозначенный символом Ох отвечает за окисление при условии, что молекула субстрата предварительно была правильно ориентирована при ее иммобилизации на поверхности фермента. Правильная ориентация возможна лишь в том случае, если между поверхностью фермента и молекулой лимонной кислоты, содержащей энантиотопные группы, осуществляется трехточечный контакт тремя группами СООН. [9]
При ферментативном окислении молекул биологического топлива отщепляется обычно по два восстановительных эквивалента и каждый атом кислорода присоединяет к себе тоже два восстановительных эквивалента. Поэтому единицей биологического окисления принято считать перенос одной пары восстановительных эквивалентов от субстрата на кислород. [10]
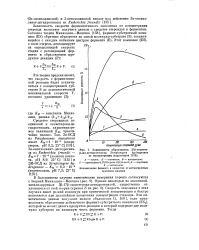 |
Зависимость образования 20 3-окспсте. [11] |
Зависимость скорости ферментативного окисления от концентрации стероида позволяет получить данные о сродстве стероидов к ферментам. [12]
Проанализирована роль ферментативного окисления к-алканов в эмульсиях при микробиологическом синтезе белковых веществ. [13]
Такая последовательность ферментативного окисления гидроксиль-ных групп ( XIV) не является единственно возможной. Streptomyces gelatieus [55], например, окисляет сначала За -, а затем 12а - оксигрушгы ( аналогично химическому окислению по Оппенауэру [56 ] или дегидрированию никелем Ренея [57]), тогда как Aspergillus niger [58], по-видимому, окисляет в первую очередь 12а - оксигруппу. [14]
Сорбоза получается ферментативным окислением D-сорбита, встречающегося в значительном количестве в ягодах рябины. Промышленным источником D-сорбита служит D-глюкоза, переходящая в него при восстановлении. Эти методы синтеза описываются ниже. [15]
Страницы: 1 2 3 4