Известный окислитель
Cтраница 1
Известные окислители, которые еще более значительно отличаются по своим свойствам от первых трех, как, например, фтор и окислители на основе соединений фтора. [1]
Наиболее известными окислителями являются концентрированная азотная кислота HNO3, насыщенная окислами азота ( NO, NO2 и др.), концентрированная перекись водорода Н2О2, жидкий кислород, тетранитрометан C ( NO2) 4 и др. Все перечисленные окислители в той или иной степени ядовиты и при нарушении правил обращения с ними могут стать источником тяжелых отравлений. [2]
Хорошо известным окислителем также является белильная известь СаОС12, представляющая собой смешанную соль соляной и хлорноватистой кислот. [3]
Таким образом из всех известных окислителей перекись водорода является самым сильным. Отсюда вытекает, что отбеливающие свойства ее исключительно велики, чистота отбелки особенно высока, а продолжительность процесса мала. Вряд ли можно ожидать, что в ближайшее время удастся найти более эффективное отбеливающее средство, чем активный кислород. [4]
Перксенат-ион ХеО - - самый сильный из известных окислителей. [5]
Жидкий фтор является самым сильным из всех известных окислителей. [6]
Сульфид-ион - очень эффективный восстановитель и окисляется большинством известных окислителей. [7]
Недавно французской фирмой был заявлен в Германии патент, использующий в качестве окислителя метальной группы уже известный окислитель МпО2 в среде серной кислоты. Мы только-что упоминали этот прием окисления применительно к получению альдегида. Оказывается, если вести процесс при температуре свыше 40 ( преимущественно при 60 - 70), то в продукте окисления преобладает бензойная кислота. [8]
Вещество парамагнитно ( Мэфф 2 57), бурно реагирует с водой и является одним из сильнейших известных окислителей. [9]
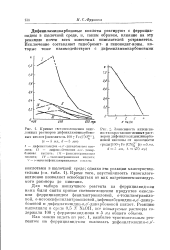 |
Кривые светопоглощения окисленных растворов дпфенилампнкарбоно-вых кислот [ окислитель 100 -у Fe ( CN3 - ]. [10] |
Дифениламинкарбоновые кислоты реагируют с феррициа-нидом в щелочной среде, и, таким образом, влияние на эту реакцию почти всех известных окислителей устраняется. [11]
Характерной особенностью фторид-ионов является их неспособность окисляться под действием химических агентов до свободного F2, так как последний является наиболее сильным из всех известных окислителей. [12]
Помимо указанных выше реакций гидроксидные радикалы образуются также при радиолизе воды и в низких концентрациях обычно присутствуют в водных растворах. ОН из всех известных окислителей является самым сильным, вызывающим радиационные повреждения многих типов биополимеров. [13]
Это довольно устойчивое соединение, разлагается только при 300 С. Ион ХеОв ( р) - самый сильный из известных окислителей. [14]
В основном окислительно-восстановительные реакции имеют сравнительно высокую мольную теплоту и, следовательно, могли бы очень легко применяться в термометрическом анализе, однако очень немногие исследователи применяют термометрический метод для анализа окислительно-восстановительных систем. Несмотря на то, что возможность использования реакций большинства наиболее известных окислителей и восстановителей в термометрическом анализе изучена, однако применение их не получило широкого распространения. [15]
Страницы: 1 2