Известный окислитель
Cтраница 2
Это довольно устойчивое соединение, разлагается только при 300 С. Ион ХеОб - ( р) - самый сильный из известных окислителей. [16]
Главная подгруппа этой группы содержит галогены - элементы F, Cl, Br, I, At. Первый элемент подгруппы галогенов-фтор - является самым сильным из всех известных окислителей. Водный раствор HF является кислотой средней силы. [17]
Главная погруппа этой группы содержит галогены - элементы F, Cl, Br, I, At. Первый элемент подгруппы галогенов - фтор - является самым сильным из всех известных окислителей. HF в водном растворе является кислотой средней силы. [18]
Большое число различных реагентов вызывает окислительное декарбоксилирование а-аминокислот. Например, использование пиколината серебра ( II) [68] количественно дает альдегиды; к тем же изменениям могут приводить и такие более известные окислители, как N-бромсукцинимид и гипохлорит. Эти реакции, по-видимому, протекают в широком смысле по одному пути через имин, который гидролизуется с образованием аммиака и альдегида. В этом случае образование основания Шиффа приводит к таутомерному сдвигу и декарбоксилированию, в конечном итоге приводящему к альдегиду, аммиаку и восстановленному карбонильному соединению. [19]
Пероксид водорода как окислитель обладает важным достоинством: он не загрязняет обрабатываемый материал другими, посторонними, продуктами разложения. Особое достоинство Н2О2 заключается еще и в том, что благодаря своему высокому окислительному потенциалу и большому количеству выделяющейся при разложении энергии, он является сильным окислителем, значительно превосходящим по силе все другие известные окислители. [20]
Рассмотренные нами особенности окислительно-восстановительных реакций, а также приведенные в табл. 3 Приложения потенциалы относятся к процессам, протекающим в водных растворах. Но вода, как реакционная среда, сама обладает окислительно-восстановительными свойствами. Например, фтор - сильнейший из известных окислителей, нельзя применять в водных растворах, так как он взаимодействует с водой с выделением кислорода, а такие сильные восстановители, как щелочные металлы, выделяют из воды водород. Однако такие реакции разложения воды практически протекают настолько медленно, что их приходится учитывать только при длительном хранении водных растворов окислителей или восстановителей. Медленность протекания некоторых окислительно-восстановительных реакций - причина того, что в отдельных случаях практически не происходит взаимодействия между веществами с большой разностью окислительно-восстановительных потенциалов. [21]
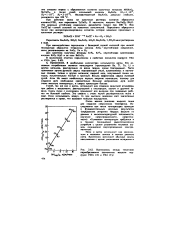 |
Взаимосвязь между теплотами парообразования элементных веществ подгрупп VIIIA О и VIIA ( Гг. [22] |
При действии озона на щелочные растворы ксенатов образуются к сенаты ( VIII), или перксенаты Э ХеОб. Это довольно устойчивое соединение, разлагается только при 300 С. Ион ХеО - р) - самый сильный из известных окислителей. [23]
На стадии лабораторных исследований находится метод прямого окисления ортанических загрязнений производственных стоков - окисление озоном. Применение озона не связано с расходом привозных реагентов; производство его может быть организовано на месте при наличии озонаторной установки и электроэнергии. Для очистки промышленных сточных вод озон более удобен, чем другие известные окислители, в том числе активный хлор. [24]
Жидкий фторид водорода является уникальным ионизирующим растворителем. Он практически не проявляет окислительных и восстановительных способностей. В отличие от других галогеноводо-родов HF не окисляется ни одним из известных окислителей до элементного фтора, поэтому его можно применять для приготовления растворов любых окислителей и в его среде успешно проводить титрование по редокс-методу. [25]
Пары ее обладают резким запахом и сильно ядовиты. В отличие от других галогеноводородных кислот, HF представляет собой кислоту средней силы. Другая особенность ее заключается в неспособности ионов F - окисляться до свободного F2, так как последний является наиболее сильным из всех известных окислителей. Кроме того, фторид серебра AgF хорошо растворим в воде, в то время как AgCl, AgBr и AgJ в ней практически нерастворимы. [26]
Ион F является анионом фтористоводородной кислоты HF, представляющей собой летучую жидкость, кипящую при 19 4 С, Пары ее обладают резким запахом и сильно ядовиты. Особенность ее заключается в неспособности F - окисляться под действием химических реагентов до свободного F2, так как фтор является наиболее сильным из всех известных окислителей, Другое отличие от этих кислот состоит в том, что фторид серебра AgF хорошо растворим в воде, в то время как AgCl, AgBr и Agl в ней практически нерастворимы. [27]
Фтор является одним из самых реакционно способных элементов. Это делает его весьма перспективным ракетным окислителем. Он является самым сильным из всех известных окислителей. [28]
Из продуктов взаимодействия ЭРв с различными веществами наиболее интересны производные молекулярного кислорода и ксенона. Красные кристаллы OjIPtFej могут быть получены прямым взаимодействием сухого О2 с PtF6 при обычных условиях. В вакууме выше 90 С эти кристаллы возгоняются, а в запаянной трубке плавятся при 219 С. Для структурных параметров молекулы найдены значения d ( PtF) 1 74 А ( по другим данным - 1 82А) и d ( OO) 1 13 А. Вещество парамагнитно ( Мефф 2 57), бурно реагирует с водой и является одним из сильнейших известных окислителей. [29]
Страницы: 1 2