Более сильный окислитель
Cтраница 1
Более сильные окислители, чем иод, окисляют тиосульфат в сульфат. [1]
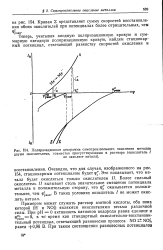 |
Поляризационная диаграмма самопроизвольного окисления металла двумя окислителями, совместно присутствующими в растворе ( окислитель. [2] |
Более сильный окислитель / / вызывает столь значительное смещение потенциала металла в положительную сторону, что ф оказывается положи-тельнее, чем Фравн. В таких условиях окислитель / не может окислять металл. [3]
Более сильные окислители в некоторых случаях превращают а-оксикислоты в карбоновые кислоты, содержащие на один атом углерода меньше. Хлорид карнитина ( - хлортриметиламино-а-оксимасля-ная кислота) при действии перманганата кальция превращается в гомобетаин 1083: С1 - ( CHS) 8N - СН8 - СН2 СНОН СООН - - Cl - ( CHS) 3N СН2 СНа - СООН. [4]
Более сильные окислители ( например, концентрированная ТШО3) превращают в карбоксил не только альдегидную, но и первичную спиртовую группу, причем образуются двухосновные кислоты. [5]
Более сильные окислители ( например, концентрированная НМО3) превращают в карбоксил не только альдегидную, но и первичную спиртовую группу, причем образуются двухосновные кислоты. [6]
Более сильными окислителями сама двуокись марганца может быть окислена в соединения с более высокой валентностью марганца. [7]
 |
Схема контактной камеры озонирования сточных вод. [8] |
Более сильным окислителем, чем хлор, является озон. Он обладает способностью разрушать в водных растворах при нормальной температуре многие органические вещества и примеси. По сравнению с хлором и другими окислителями озон имеет ряд преимуществ. [9]
Более сильными окислителями, чем пероксиды и надпероксиды, являются озониды. [10]
Более сильным окислителем является смесь концентрированных азотной и соляной кислот - царская водка. Она растворяет даже золото и платину, которые не растворяются в азотной и тем более в соляной кислоте. [11]
Чем более сильный окислитель участвует в реакции, тем выше поднимается степень окисления восстановителя. [12]
Хотя более сильные окислители превращают N-монозамещен-ные гидроксиламины в С-нитросоединения [91], реакции этого типа не имеют сколько-нибудь существенного значения для орга нического синтеза. Окисление Ы Ы - дизамещенных гидроксилами-нов может приводить к образованию производных двух типов в зависимости от природы заместителей при углеродных атомах, соединенных с атомом азота. Более подробно реакции этого типа рассмотрены в разд. [13]
Еще более сильным окислителем, чем кислород, является озон. [14]
Озон - более сильный окислитель, чем кислород, так как он разлагается с выделением атомного кислорода. [15]
Страницы: 1 2 3 4