Окись - кремний
Cтраница 1
Окись кремния ( монокс) - это тонкодисперсный буро-каштановый порошок. [1]
Окись кремния SiO2 ( кремнезем) обладает сильными кислотными свойствами и нерастворимостью в железе, легко вступает в комплексные соединения с основными окислами. С закисью железа образует нерастворимый в металле силикат закиси железа FeO - SiO2, легко всплывающий в шлак. [2]
Окись кремния ( 5Ю) - аналог окиси углерода - не существует в природе. Ее синтезируют из смеси кремния и песка. Полимер медленно окисляется на воздухе, а при 400 - 700 разлагается на кремний и двуокись кремния. [3]
Окись кремния и окись алюминия в определенном сочетании значительно активнее каждого компонента в отдельности. [4]
Окись кремния ( силикагель) и окись алюминия, каждая в отдельности, обладают небольшой каталитической активностью по сравнению с активностью смешанного алюмосиликатного катализатора, приготовленного из этих окислов. Активность смешанного катализатора намного превосходит сумму активностей компонентов. [5]
Окись кремния в железе нерастворима и всплывает в шлак. Кремний образует с основными окислами комплексные, легко всплывающие соединения, нерастворимые в металле. [6]
Окись кремния ( 1У) ( кремнезем) часто встречается в природе как в чистом виде, так и в составе многих пород. Окись кремния ( ТУ) существует в трех полиморфных кристаллических модификациях, а также в различных аморфных и микрокристаллических формах. Три кристаллические модификации - кварц, тридимит и кристобалит - с очень большим трудом превращаются друг в друга. Это видно из того, что последние две модификации, несмотря на свою неустойчивость при обыкновенной температуре, могут неограниченное время существовать в природе в виде минералов. [7]
 |
Схематическое изображение кристаллической и стекловидной форм гипотетического соединения М2О3. [8] |
Окись кремния ( 1У) очень устойчива по отношению к химическим реагентам. При комнатной температуре на нее действует лишь фтористоводородная ( плавиковая) кислота ( стр. В воде окись кремния ( 1У) практически нерастворима. На холоду на нее не действуют и основания. Сплавлением с едким натром и едким кали получают соответственно силикаты натрия и калия. Эти силикаты образуются также при сплавлении окиси кремния ( 1У) с карбонатами щелочных металлов: одновременно происходит выделение двуокиси углерода. Аналогично силикаты образуются и при сплавлении окиси кремния ( 1У) с другими основными окисями. Более реакционноспособным, чем кварц, является силикагель, который растворяется также в растворах щелочей. Следовательно, окись кремния ( 1У) ведет себя как ангидрид кремневой кислоты. Очень низкая реакционная способность окиси кремния ( 1У) обусловлена макромолекулярной структурой. Чистый прозрачный кварц используется для изготовления линз и призм, пропускающих ультрафиолетовый свет. Для аналогичных целей используют также кварцевое стекло. [9]
Окись кремния из полученного раствора осаждают соляной кислотой. Для этого приливают 10 - 15 мл концентрированной соляной кислоты и прикрывают чашку часовым стеклом во избежание разбрызгивания раствора. Затем чашку ставят на водяную баню и содержимое выпаривают досуха. Сухой остаток вновь смачивают 15 мл концентрированной соляной кислоты и выпаривают. Процесс добавления соляной кислоты и выпаривания повторяют еще раз. После охлаждения добавляют 15 мл концентрированной соляной кислоты и ставят на водяную баню для коагуляции кремневой кислоты. [10]
Окись кремния в сочетании с окислами различных других элементов образует ряд весьма разнообразных систем, которые служат материалом для изготовления цемента, огнеупоров, керамики, стекол, катализаторов или подкладок для катализаторов. Изучению структур силикатов посвящено очень много работ, в которых используются разнообразные методы, в том числе и методы физико-химического анализа. Диаграммы состояния силикатных систем бывают очень сложны вследствие образования ряда промежуточных соединений из основных компонентов системы и вследствие способности многих соединений, а также и исходных компонентов переходить по мере охлаждения от одной кристаллической модификации к другой. Кроме того, в силикатных системах нередко образуются твердые растворы. [11]
Окись кремния и сульфаты металлов, содержащиеся в катализаторе, снижают его активность. Катализаторы конверсии отравляются под действием сернистых соединений, в частности сероводорода [223, 224], в связи с превращением никеля в соответствующие неактивные соединения - сульфаты и сульфиды никеля. На свойства катализаторов существенно влияют качество применяемого сырья и условия их приготовления. [12]
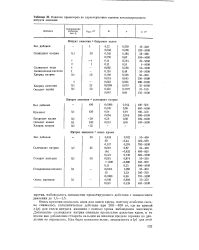 |
Влияние промоторов на характеристики горения катализированного нитрата аммония. [13] |
Окись кремния оказалась ядом для окиси хрома, поэтому особенно сильно снижалось каталитическое действие при 200 - 400 ат, где на кривой и ( р) для смеси нитрата аммония с окисью хрома наблюдался максимум. [14]
Окись кремния вводилась как инертная добавка для снижения температуры взрыва, о возможной ее роли в механизме ингибировапия будет сказано ниже. [15]
Страницы: 1 2 3 4