Окись - бутилен
Cтраница 1
Окиси бутилена ( 1 2-эпоксибутан и 2 3-эпоксибутан) используются для производства бутиленгликолей и их производных, а также для получения поверхностно-активных агентов. Эпихлоргидрин применяется в качестве химического промежуточного звена, инсектицида, фумиганта и растворителя для красок, лаков, эмалей и лаков для ногтей. Он также входит в состав полимера, применяющегося для покрытия водопроводных труб, и служит сырьем для производства смол для пропитки влагопрочной бумаги. [1]
Окиси бутиленов получаются переводом. [2]
При обработке окиси симметричного бутилена раствором НС1 получают единственное соединение А. Кинетика подчиняется уравнению третьего порядка, скорость реакции зависит от концентраций кислоты и окиси. Зная, что при увеличении концентрации окиси в 2 раза скорость реакции также возрастает вдвое, приведите механизм реакции и стереохимию продукта конденсации. [3]
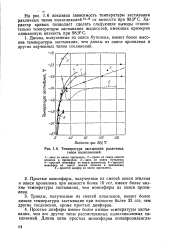 |
Температура застывания различных типов полигликолей. [4] |
Диолы, полученные из окиси бутилена, имеют более высокие температуры застывания, чем диолы из окиси пропилена и других изученных типов соединений. [5]
 |
Показатели сопряженного окисления с получением окисей олефинов. [6] |
Общеизвестным является хлоргидринный метод получения окиси бутилена, основанный на тех же реакциях, что и получение окисей этилена и пропилена. [7]
В настоящее время налажено производство окисей бутилена путем хлоргидринирования олефинов и дегидрохлорирования получаемых бутилен-хлоргидринов. [8]
Кроме того, получены полимеры из окисей бутилена, окиси стирола и эпихлоргидрина. [9]
Если в качестве окислителя используется надуксусная кислота, то одновременно с окисью бутилена образуется уксусная кислота. Известно, что окисление олефинов в а-окиси надуксусной кислотой применяется в США при промышленном получении эпоксидных смол. Однако осуществление этого процесса в промышленных условиях сопряжено с трудностями, связанными с взрывоопасностью процесса. [10]
Используя такие инициаторы, как моно -, ди - и трипен-таэритрит и тетраметилолциклогексан, Де-Гроте и Пет - тингилл68 получили сополимеры окисей бутилена и этилена, а также окисей бутилена, этилена и пропилена. [11]
Используя такие инициаторы, как моно -, ди - и трипен-таэритрит и тетраметилолциклогексан, Де-Гроте и Пет - тингилл68 получили сополимеры окисей бутилена и этилена, а также окисей бутилена, этилена и пропилена. [12]
Таким же образом могут быть подвергнуты взаимодействию в автоклаве: 150 г желатины, 242 г цетилового спирта, 72 г масляного альдегида с 440 г окиси этилена; 100 г мездрового клея, 240 г пальмитинового альдегида с 720 г окиси бутилена; 120 г мочевины, 298 г рицинолевой кислоты и 224 с сорбиновой кислоты с 880 г окиси этилена. [13]
Подобным же образом можно приготовить ив окиси этилена и метанола монометиловый эфир этиленгликоля с 85 % - ным выходом; из окиси 1 2-пропилена и этилового спирта получается с 85 % - ным выходом моноэтиловый эфир 1 2-пропиленгликоля, а из окисей бутилена и этилового спирта - моноэтиловый эфир бутиленгликоля. [14]
Выход целевого продукта достигает 43 мол. Окись бутилена выделяют из продуктов реакции фракционированием при 50 - 60 С. Побочно образуется небольшое количество метилацетата, уксусного и крото-нового альдегидов, метилэтилкетона и кислот - муравьиной, уксусной, пропионовой. Последние удаляют содовой промывкой. [15]
Страницы: 1 2