Окись - скандий
Cтраница 1
Окиси скандия соответствуют интенсивная система полос в оранжевой области и более слабая система в сине-зеленой. [1]
Окись скандия, выделенная при переработке урановой руды, за счет изотопа тория была радиоактивной, что создавало дополнительную проблему при получении продукта высокой степени чистоты. [2]
Окись скандия образуется при прокаливании гидроокиси, карбоната, нитрата или оксалата скандия. [3]
Очищенную окись скандия еще раз растворяют в соля пой кислоте и щавелевой кислотой осаждают оксалат скан дня. [4]
Очищенную окись скандия еще раз растворяют в соляной кислоте и щавелевой кислотой осаждают оксалат скандия. Его прокаливают при 1100 С и превращают в окись. [5]
Поскольку окись скандия в несколько раз дешевле чистого металла, со применение в некоторых случаях моглс бы оказаться экономически оправданным. [6]
Поскольку окись скандия в несколько раз дешевле чистого металла, ее применение в некоторых случаях могло бы оказаться экономически оправданным. [7]
Механизм растворения окиси скандия, имеющей кубическую структуру типа Мп2Оз, в сложном окисле Ca3UO6 с ромбически искаженной структурой типа криолита, столь отличной от Mn2O3, на первый взгляд кажется необъяснимым. [8]
Применявшаяся для опытов окись скандия была получена из тиосульфата скандия и проверена рентгеноспектральным анализом. Окислы редких земель были проверены на чистоту таким же путем. [9]
Применявшаяся для опытов окись скандия была получена из тиосульфата скандия и проверена рентгеноспектрально. Окислы редкоземельных элементов были проверены на чистоту таким же путем. [10]
Для этой цели от окиси скандия, полученной после прокаливания осажденной гидроокиси ( однократное отделение), отбирали 1 0 мг и определяли в этом количестве примесь окислов редкоземельных металлов рентгеноспектральным методом. [11]
Такое увеличение параметра решетки окиси скандия в образцах можно объяснить только растворимостью в ней Ca3UOe; так как образец с 90 % Sc2O3 содержит в себе и Sc2O3, и Са3иО6 - тв. [12]
Для опытов точные навески окиси скандия и окислов редкоземельных металлов растворяли при нагревании в концентрированной азотной кислоте и избыток кислоты удаляли осторожным упариванием. Что касается церия, то был изготовлен титрованный раствор Ce ( NO3) 2 6Н2О, титр которого был установлен весовым путем. [13]
Для опытов точные навески окиси скандия и окислов редкоземельных металлов растворяли при нагревании в концентрированной азотной кислоте, и избыток кислоты удаляли осторожным упариванием. Что касается церия, то титрованный раствор приготовляли, исходя из Се ( МО3) з - 6Н2О, титр которого был установлен весовым путем. [14]
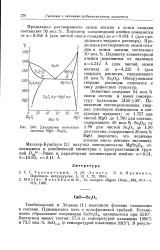 |
Диаграмма состояния системы MgO - Sc203. [15] |
Страницы: 1 2 3 4