Окись - хлор
Cтраница 1
Окись хлора представляет собой взрывчатый желто-бурый газ с запахом, похожим на запах хлора. [1]
Окись хлора разлагается также при действии солнечного овета; этот процесс протекает в течение нескольких минут. [2]
Окись хлора можно хранить в сжиженном состоянии при температуре - 80 С; при этом разложение ее не наблюдается в течение длительного времени. При температуре около - 20 С жидкая окись хлора разлагается через несколько дней. [3]
Окись хлора - одно из наиболее реакционноспособных соединений; несмотря на возможность взрывов при работе с этим веществом, осе же при определенных условиях оно может применяться для целей хлорирования. [4]
Окиси хлора соответствует хлорноватистая кислота НС1О; хлорному ангидриду - хлорная кислота НСЮ; двуокись хлора, реагируя со щелочами, образует соли двух кислот: хлорноватой НСЮз и хлористой НС. Из кислородных соединений хлора наибольшее практическое значение имеют соли хлорноватистой и хлорноватой кислот. Они получаются действием хлора на растворы щелочей. [5]
Окись хлора можно хранить в сжиженном состоянии при температуре - 80 С; при этом разложение ее не наблюдается в течение длительного времени. При температуре около - 20 С жидкая окись хлора разлагается через несколько иней. [6]
Окись хлора, соответствующая белильным и хлорноватистым, солям, содержа в себе два элемента, кислород и хлор, действующие оба окислительным образом, представляет характерный пример соединения элементов, которые химически действуют в большинстве случаев сходственным образом и прямо друг на друга не реагируют. В безводном виде ( газ или жидкость) легко взрывает, разлагаясь на С12 и О. Взрыв может происходить даже случайно, а также от присутствия многих окисляемых веществ ( напр. [7]
Окись хлора считается более сильным окислителем, чем хлорноватистая кислота5; это подтверждается тем, что жидкая окись хлора при переливании разлагается со взрывом. [8]
Окись хлора разлагается также при действии солнечного света; этот процесс протекает в течение нескольких минут. [9]
Окись хлора является одним из наиболее энергичных реагентов и бурно реагирует с органическими веществами. При соприкосновении с каучуком или скипидаром газообразная окись хлора взрывает. Взаимодействие окиси хлора с органическими веществами в препаративных целях мало изучалось. [10]
Окиси хлора соответствует хлорноватистая кислота НСЮ; хлорному ангидриду - хлорная кислота НСЮ4; двуокись хлора, реагируя со щелочами, образует соли двух кислот: хлорноватой НСЮ, и хлористой НСЮ. Из кислородных соединений хлора наибольшее практическое значение имеют соли хлорноватистой и хлорноватой кислот. Они получаются действием хлора на растворы щелочей. На эту реакцию большое влияние оказывает температура. При действии хлора на раствор щелочи на холоду получаются соли хлорноватистой и соляной кислот. [11]
Окись хлора легко взрывает при переливании ее в жидком состоянии из одного сосуда в другой, а также при нагревании или соприкосновении с горючими веществами. [12]
Окись хлора хорошо растворима в четыреххлористом углероде, и ее можно хранить в виде такого раствора. Существование свободной окиси иода 120 весьма сомнительно. [13]
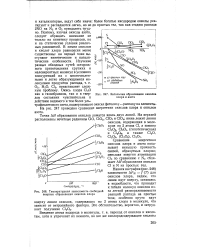 |
Энтальпии образования окислов хлора и азота.| Температурная зависимость свободной энергии образования окислов хлора. [14] |
Окись хлора С12О как в газообразном, так и в твердом состоянии чувствительна к действию видимого и тем более ультрафиолетового света, подвергающего окисел фотолизу-распаду на элементы. На рис. 247 приведено сравнение энергетики окислов хлора и окислов азота. [15]
Страницы: 1 2 3 4