Окись - церие
Cтраница 1
Окись церия в количестве 100 г помещают в фарфоровую чашку емкостью 1000 мл, прибавляют 250 мл серной кислоты ( 1: 1) и нагревают при температуре 120 - 130 до тех пор, пока нерастворившаяся масса не примет ярко-желтого цвета. Нерастворившийся осадок отфильтровывают и устанавливают титр раствора по соли Мора. [1]
Окись церия, добываемая из церита, содержит около 40 % другого основания, которое несравненно сильнее, нежели окись церия, от которой ее отделяют растворением в весьма слабой кислоте. Понимается, что для этого нужно, чтобы церий был совершенно превращен в состояние окиси и прокален докрасна. [2]
Окись церия ( IV) полу чается после прокаливания гидроокиси церия ( IV) при 500 С и оксалата церия ( IV) при 800 С. [3]
Окись церия ( IV) получается после прокаливания гидроокиси церия ( IV) при 500 С и оксалата церия ( IV) при 800 С. [4]
Окись церия в смеси со SrO используется в производстве специальных радиокерамических материалов. При изготовлении электронных ламп редкоземельные элементы служат превосходными поглотителями газов - так называемыми геттерами. [5]
Окись церия используется в качестве абразивного материала, особенно для шлифовки оптического стекла. [6]
Окись церия ( IV) получается после прокаливания гидроокиси церия ( IV) при 500 С и оксалата церия ( IV) при 800 С. [7]
Однако окись церия ( 4) растворяется в кислотах исключительно медленно. Ее можно превратить в безводный сульфат нагреванием с концентрированной серной кислотой или восстановить до церия ( 3) и действием перекиси водорода или иодидов щелочных металлов в кислой среде перевести в растворимую форму. [8]
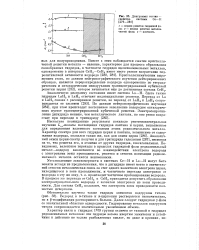 |
Диаграммы состав - свойство системы Се-II. [9] |
Аналогичный окиси церия спектр получен и для тригидрида гадолиния [287], несмотря на то, что решетка его, в отличие от других гидридов, гексагональная. По-видимому, валентные переходы в пределах гидридной фазы редкоземельный металл-водород заключаются во взаимодействии электрона водорода с электронами зоны проводимости, решетка и степень ионизации редкоземельного металла остаются неизменными. [10]
Гидраты окиси церия ( IV) растворяются гораздо легче. Горячая концентрированная серная кислота полностью растворяет двуокись церия с образованием желтого сульфата церия. Разбавленная серная кислота не оказывает заметного действия на окись. Соли других кислот легко получаются действием соответствующих кислот на гидроокиси при анодном окислении соответствующих солей церия ( III) ( см. статью Некерса и Кремерса [207] с описанием анодного окислительного процесса) или путем окисления персульфатом, двуокисью свинца, висмутатом натрия, азотной кислотой. [11]
Соли окиси церия по своей окислительной способности приближаются к перманганату. Этим свойством пользуются для количественного определения некоторых окисляющихся веществ. [12]
Порошки из окиси церия широко применяются при полировке оптических стекол. В производстве специально окрашенных технических и декоративных стекол используются окиси церия, неодима и празеодима, которые увеличивают светопрозрачность и способность стекла пропускать инфракрасные лучи. Введение окиси церия делает стекло способным поглощать ультрафиолетовые лучи. [13]
Для отделения окиси церия от окиси лантана смесь окислов растворяют в небольшом количестве концентрированной азотной кислоты. При разбавлении большим избытком горячей воды вследствие гидролиза выпадает осадок гидроокиси церия, который отфильтровывается. Фильтрат содержит в основном гидроокись лантана. [14]
В аналогичных условиях окись церия СеО2 активности не проявляет. Ряды активности катализаторов гидрирования пропилена и этилена в общем совпадают. Исключение составляет La2O3, которая при низкотемпературном гидрировании оказалась значительно активнее остальных окислов. Возможно, это связано с предварительной обработкой контактов, проводимой при низкотемпературном гидрировании. [15]
Страницы: 1 2 3 4