Окись - элемент
Cтраница 1
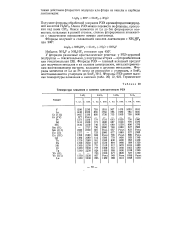 |
Температура плавления и кипения тригалогенидов РЗЭ. [1] |
Окиси элементов от La до Sm фторируются полностью, остальные в разной степени, степень фторирования понижается с увеличением порядкового номера лантаноида. [2]
В сублиматах окисей элементов группы IV-A в парах присутствуют как двуокиси, так и моноокиси, причем последние в общем имеют меньшее значение, чем первые. Процессы сублимации окислов элементов V - 4 и VI-A групп более сложны. Здесь обычно, налицо более чем одна конденсированная фаза и более сложен состав газовых молекул. Состав паров пятиокисей ванадия и тантала сильно различается, хотя эти два элемента являются аналогами. Так, пятиокись ванадия, испаряясь, образует преимущественно сложные молекулы: V4010, V408, V6014, Ve012 и V204, в то время как пятиокись тантала дает в восстановительных условиях газообразные двуокись и моноокись, а в нейтральных - двуокись и кислород. [3]
Мы предполагаем, что окиси элементов группы Va и Via дают возможность устранить стерические факторы в соединениях элементов этой части периодической таблицы, поэтому очень жаль, что по стабильности координационных соединений этих окисей имеется очень мало сведений. Правда, учитывая возросший в последнее время интерес к исследованиям в этой области [70, 359], можно ожидать, что такая информация должна появиться в ближайшем будущем. [4]
Как изменяются свойства гидратов окисей элементов подгруппы германия от германия к свинцу. [5]
Имея высокие температуры плавления, окиси элементов этой подгруппы являются превосходными тугоплавкими материалами. [6]
Как должны меняться свойства гидратов окисей элементов данной группы. [7]
В каком направлении усиливаются основные свойства гидратов окисей элементов главной подгруппы второй группы и чем это можно объяснить. [8]
Окись бериллия дает основание менее энергичное, чем все прочие окиси элементов этой группы: энергия возрастает с возрастанием атомного веса. [9]
VI мы обсудим те немногие данные, которые известны об основности окисей фосфинов в сравнении с окисями элементов V и VI групп. [10]
Найденное содержание Rt2O ( Cs2O) в растворе пробы в мкг / мл, деленное на 50, дает процентное содержание окисей элементов в образце. [11]
Многочисленные расплавленные окиси, гидроокиси, соли и смеси солен оказывают корродирующее действие на платиновые металлы. Такое же действие оказывают расплавленные перекиси, гидроокиси и нитраты элементов la группы и ] окиси элементов Па группы; сильнее всего действуют смеси гидроокисей и карбонатов или нитратов элементов 1а группы. Расплавленные цианиды щелочных металлов также действуют на платиновые металлы. [12]
Коровин и Л. В. Липнс р34 ] показали, что анализ в полом катоде может быть с успехом использован при определении целого ряда примесей в труднолетучих основах, давая результаты, иногда лишь немногим уступающие тем, которые дают разработанные для этой цели методы фракционной дистилляции с носителем и метод испарения ( см. гл. В цитированных работах изложено применение полого катода к анализу окиси циркония, которая выбрана как типичный пример окиси элемента со сложным спектром, имеющей малую упругость паров. [13]
Из окисей, исследованных Гернет и Хитун [106] ( окиси кальция, магния, стронция, цинка, алюминия, висмута, марганца, никеля, кобальта и меди), не все оказались промоторами при добавлении к катализатору Сг203 - 8пОг, употребляемому при каталитическом окислении двуокиси серы. Окись бария и окись железа ясно активировали катализатор. Для окисей элементов с четным атомным числом наблюдается меньшее отрицательное влияние, чем для элементов с нечетными атомными числами. [14]
Ошибку в определении можно ждать еще и потому, что в чистоте препаратов нет возможности убедиться чем-либо иным, как многократною кристаллизациею, а она, как известно, не всегда служит для отделения от изоморфных подмесей. Это место III-8 должно отвечать, судя по атоманалогии с Gs, Ва-Се, элемеиту, дающему [ резкое ] ясное основание и мало летучие хлористые соли, что подходит под свойства как дидимия, так и лантана. Третье свободное место есть еще в V группе в 12 ряде между Th 231 и Ur 240 для элемента, дающего R205 и обладающего атомным весом около 235, следовательно эквивалентом около 49, но это место едва ли принадлежит одному из наших металлов, потому что эквивалент очень высок, и окись элемента, стоящего на этом месте, должна быть сравнительно слабым основанием, менее энергическим, чем ThO2, но более ясным, чем U03, а в окисях лантана и дидима основные свойства развиты очень ясно, они и после прокаливания растворяются в слабых кислотах. Окись и металл этого места должны быть тяжелы, судя по свойствам атоманалогов и чего нет в окисях Di и La, уд. Поэтому я думаю, что La и Di принадлежат к двум первым упомянутым местам, то-есть окись одного имеет состав R203, а другого R02, одна отвечает низшей, а другая высшей форме окисления церия. [15]
Страницы: 1 2