Окись - галлий
Cтраница 3
Незначительные добавки окиси галлия заметно влияют на свойства окисей многих металлов. Так, примесь Ga203 к окиси цинка значительно уменьшает ее спекаемость. [31]
Реакция с окисью галлия идет при температуре выше 600 С. Но для достаточно интенсивного протекания реакции температуру приходится повышать до 1000 - 1200 С. [32]
Для изучения влияния окиси галлия на термические условия зоны разряда нами [2] была измерена температура плазмы дуги при сжигании окислов РЗЭ в отсутствие и в присутствии окиси галлия. [33]
Малая растворимость гидратов окисей галлия и индия ( произведение растворимости равны соответственно 10 - 33 и 10 - 33) и относительно малая величина рН начала осаждения позволяют предположить, что механизм соосаждения галлия и индия, по-видимому, заключается в механическом захвате осадком фосфата кальция золей гидроокисей галлия и индия. Поскольку гидроокись галлия амфотерна и заметно растворима в аммиаке, мы наблюдаем падение процента соосаждения галлия с повышением значения рН раствора; этого явления не наблюдается для индия. [34]
Система окись алюминия - окись галлия - вода. [35]
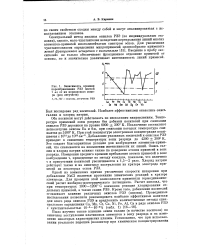 |
Зависимость времени парообразования РЗЭ массой 1 м г от их порядкового номера ( ряд летучести. [36] |
Было изучено также влияние окиси галлия ( в качестве носителя) на кинетику поступления платиновых элементов в зону разряда и на изменение некоторых характеристик плазмы. [37]
Результаты определения основного вещества в окиси галлия по вышеописанному методу помещгны в таблице. [38]
Полученная при невысоких температурах, окись галлия растворяется в кислотах, образуя соли галлия, и в щелочах, образуя галлаты. Для перевода прокаленной окиси в растворимую форму приходится сплавлять ее со щелочью. [39]
Пусть добавляем в кристалл ZnO окись галлия, так что материал становится n - типа, с ионами, Ga3, замещающими некоторые ионы Zn2 в решетке. [40]
При применении в качестве носителя окиси галлия значительно повышается интенсивность линий примесей в перечисленных выше редкоземельных окислах. [41]
Известны и другие способы концентрации окиси галлия из алюминатных растворов. Так, из остающегося после электролитического рафинирования алюминия по трехслойному методу анодного сплава, содержащего 0 1 - 0 3 % галлия, последний может быть выделен путем обработки сплава горячим раствором щелочи. При этом алюминий и галлий переходят в раствор, а медь и железо остаются в осадке. [42]
Оказалось, что при анализе уран-ниобиевых сплавов окись галлия образует тройное соединение с ураном и ниобием, плавящееся при нагревании в аноде дуги. При этом условия фракционирования примесей изменяются, и в зону разряда поступает заметное количество урана. [43]
Галлиевый концентрат, содержащий до 10 % окиси галлия, растворяют в соляной кислоте, и галлий экстрагируют эфиром. Концентрация соляной кислоты должна составлять около 5 5 - м, Эфирный слой отделяют и эфир удаляют выпариванием. Экстракционный метод позволяет очистить хлорид галлия от многих примесей, кроме железа, которое, как известно, также экстрагируется эфиром из солянокислых растворов. [44]
Разработана методика определения основного вещества в солях и окиси галлия обратным титрованием при рН 5 5 избытка трилона Б солью цинка в присутствии ксиленолового оранжевого. [45]
Страницы: 1 2 3 4