Магнитная окись
Cтраница 3
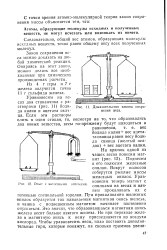 |
Опыт с железными опилками. [31] |
При прокаливании железных опилок образуется так называемая магнитная окись железа, и чашка с подвешенным магнитом начинает постепенно опускаться. Это значит, что образовавшаяся магнитная окись железа весит больше взятого железа. Но при переходе железа в магнитную окись к нему присоединяется из воздуха кислород. [32]
Скорость реакции увеличивается с повышением температуры. Повышение концентрации щелочи замедляет реакцию, так как сама реакция происходит с освобождением значительного количества щелочи. В очень сильно концентрированных щелочных растворах образование осадка магнитной окиси не наблюдается совсем. [33]
Как видно из схемы, в процессе оксидирования сталкиваются две химические реакции. Преобладающее значение каждой из них зависит от условий проведения процесса. Если окисление закис-ной формы до окисной происходит беспрепятственно, а связывание окисной формы в магнитную окись задерживается, то образуется осадок гидрата окиси железа. Окисление закисного железа до окисного ( II) идет быстро и лимитируется лишь скоростью доставки окислителя в зону реакции. Реакция образования магнитной окиси ( III) протекает сравнительно медленно, но зато выделяющаяся Fe3O4 обладает крайне низкой растворимостью, которая, однако, повышается при увеличении концентрации щелочи. Реакция образования окисного железа происходит быстро; но пересыщению раствора, а следовательно, и выделению осадка препятствует большая растворимость гидрата окиси железа. [34]
Можно представить себе такой план действий, который основан на том, чтобы исследовать каждую из простых реакций в отдельности, а затем описать явление в целом. Тогда, чтобы объяснить кинетику восстановления окиси железа Fe203, нужно будет последовательно исследовать восстановление закиси железа FeO на железе, потом восстановление магнитной окиси Fe304 и, наконец, восстановление окиси железа, используя каждый раз предыдущие результаты. [35]
Величина рН в углублении равна около 6 0 независимо от значения рН в воде вне углубления. Там, где анодно образованные железные соли встречают относительно щелочную воду, происходит выпадение осадка, образуя объемистые б у-горки не пристающей к металлу магнитной окиси; несколько дальше от металла, у границы области, где растворенный кислород имеется в избытке, появляется относительно пристающая пленка гидрата окиси железа. Иногда плейка ломается, я Сквозь отверстия прорастают бугорки, образуя над собой новую пленку. Высокие концентрации SO и СГ в углублениях, намного превышающие соответствующие концентрации в воде вне углубления, являются доказательством миграции анионов по направлению к точкам коррозии ( стр. [36]
Электролит работающих ванн всегда содержит в себе некоторое количество окисного железа, поступающего в раствор с поверхности обрабатываемых деталей. Наличие окисного железа ускоряет процесс образования магнитной окиси Fe3O4 и уменьшает толщину пленки. В этом случае образующееся около поверхности металла за-кисное железо сразу же реагирует с соединением окиси железа, уже находящимся в растворе, способствуя тем самым большему пересыщению раствора магнитной окисью. Как указывалось, большое пересыщение растворов снижает толщину образуемой пленки. Свежесоставленная ванна не дает нормального покрытия, образуя пленки большой толщины и рыхлого строения. [37]
Апокреновая к-та известна только в нерастворимой в воде форме; креповая к-та ни при каких условиях нерастворимой формы не образует. Гуминовая, ульминовая и апокреновая к-ты образуют растворимые в воде соли только с одновалентными металлами. Соли их с многовалентными металлами нерастворимы в воде; исключение составляют-только легко растворимая апокреновая соль двухвалентного железа и заметно растворимая апокреновая соль кальция. При прокаливании апокреновой соли трехвалентного железа она образует черную магнитную окись железа; те же соли ульминовой и гуминовой к-т магнитной окиси не образуют. Все без исключения соли креново & кислоты легко растворимы в воде. Растворимые соли перегнойных кислот диффундируют через коллоидную перепонку, и при условии полного освобождения их растворов от следов растворимых кремневой, титановой и кремнетитановой к-т они кристаллизуются из водных растворов. [38]
Горение нефти дает 0 446 - 9 800 4 371 Cal. Нагрев, плавление и перегрев стали требуют: 1 - 0 167 - 1 500 65 0 2 - 100336 Cal. Расход газа, дающего при сожигании 950 Cal / ж3, равен 300 ж3 на 1 m руды, содержащей 85 % магнитной окиси, из к-рых 70 % переходит в окись железа. Горение газа дает 0 3 950 285 Cal. Для нагрева руды до 800 требуется 1 - 0 223 - 800 178 4 Cal. Гофмана) для обжига известняка. Расход каменного угля 8 % от веса камня, из которого обжигом удаляется 40 % углекислоты. Горением угля дается 0 08 - 7 000 560 Cal. Выделение углекислоты требует 0 4 998 399 Cal. Горение угля дает 0 35 - 7000 2 450 Cal. Нагрев, плавление и перегрев чугуна требуют всего 0 178 1 200 4 - 23 - f 0 25 - 150 - 275 Cal. Опущено в приходе тепло окисления примесей железа и его самого, а в расходе-уносимое шлаком, что почти не меняет конечного результата расчета. [39]
Как видно из схемы, в процессе оксидирования сталкиваются две химические реакции. Преобладающее значение каждой из них зависит от условий проведения процесса. Если окисление закис-ной формы до окисной происходит беспрепятственно, а связывание окисной формы в магнитную окись задерживается, то образуется осадок гидрата окиси железа. Окисление закисного железа до окисного ( II) идет быстро и лимитируется лишь скоростью доставки окислителя в зону реакции. Реакция образования магнитной окиси ( III) протекает сравнительно медленно, но зато выделяющаяся Fe3O4 обладает крайне низкой растворимостью, которая, однако, повышается при увеличении концентрации щелочи. Реакция образования окисного железа происходит быстро; но пересыщению раствора, а следовательно, и выделению осадка препятствует большая растворимость гидрата окиси железа. [40]
Окись железа Ре Ю3 является в природе и образуется в виде красного порошка многими способами искусственно. Так, железный купорос при накаливании оставляет красную окись железа, называемую колькотаром или мумиею, употребляющуюся в виде масляной красной краски, преимущественно для окраски кровель. То же вещество в виде мельчайшего порошка употребляется для полирования стекла, стальных и других металлических предметов. Если сильно накаливать смесь железного купороса с избытком поваренной соли, то образуется кристаллическая окись железа темнофиолетового цвета, сходная с некоторыми природными видоизменениями этого вещества. Томази) легко выделяющий воду и оставляющий красную безводную окись железа. Чистая окись железа не имеет магнитных свойств, но если ее накалить до белокалиль-ного жара, то она выделяет кислород и дает магнитную окись. Безводная окись железа, накаленная до высокой температуры, растворяется с трудом в кислотах ( но в крепких растворима при нагревании, также при сплавлении с KHSO4), тогда как водная окись железа, по крайней мере та, которая осаждается из солей посредством щелочей, весьма легко растворяется в кислотах. [41]
Страницы: 1 2 3