Графитовая окись
Cтраница 2
Конечной стадией обработки графитовых частичек в кислотах является образование графитовой окиси. [16]
Формирование частичек коллоидных размеров как механическим, так и химическим диспергированием сопровождается аморфизацией кристаллической решетки. Нагревание графитовой окиси выше 135 С также приводит к проходящей через несколько стадий аморфиза-ции слоистой структуры с раздвинутыми до 0 635 - 1 16 нм 1 и неупорядоченно располагающимися углеродными гексагонами и образованию трехмерно неупорядоченного углерода с высокой степенью дисперсности. Стадии окисления графита кислотами можно проследить под электронным микроскопом, где наблюдается в процессе выдержки в смеси серной и азотной кислот исчезновение описанных выше муаровых полос, доказывающее ликвидацию графитовых кристаллитов. [17]
В природе графитовая окись может образоваться только в результате неполного окисления графитовых и карбоидных горючих ископаемых в зоне выветривания. Вследствие малой устойчивости графитовая окись обычно не накопляется в значительных концентрациях и присутствует в окисляющихся горючих ископаемых лишь как второстепенная составная часть или валяется промежуточным образованием на пути к полному окислению. [18]
В результате окисления в мягких условиях карбоиды, по крайней мере не слишком богатые углеродом, превращаются в гумусовые вещества. В более жестких условиях они дают графитовую окись, причем ее выход тем больше, чем карбоид богаче углеродом или чем выше был а температура его прокаливания. Эти реакции карбоидов устанавливают их отношение к гумусовым веществам и графитовой окиси. [19]
Графитовая окись - очень непрочное соединение и даже при слабом нагревании разлагается с выделением кислорода в виде окиси и двуокиси углерода. Следует отметить, что прокаленный нелетучий остаток графитовой окиси состоит в основном из графита. Иными словами, после удаления кислорода восстанавливаются прежние металлические связи, и графит регенерируется. [20]
В первую очередь разрываются только слабые связи между атомными слоями, сами же слои остаются нетронутыми. Таковы реакции графита с сильными окислителями при невысоких температурах, которые приводят к образованию графитовой окиси. При этом кристаллы графита набухают, теряют электропроводность и становятся прозрачными. Рентгенографическое исследование их Доказывает, что структура атомных слоев графита при этом полностью сохраняется в графитовой окиси, но расстояния между ними сильно увеличиваются. Это обусловлено тем, что кислород входит между атомными слоями и захватывает подвижные электроны, находящиеся здесь. Вследствие этого графит теряет свои металлические свойства и превращается в диэлектрик - окись графита. [21]
При очень медленном нагревании происходит самораскисление графитовой окиси. Оно заключается в постепенном отщеплении окислов углерода от краев атомных слоев. В результате чешуйки графитовой окиси Становятся меньше и теряют способность набухать. Электропроводность увеличивается, а прозрачность исчезает. Расстояния между атомными слоями уменьшаются. [22]
В составе горючих ископаемых можно обнаружить несколько на вид однородных и химически резко различных компонентов, к сочетаниям которых можно свести все ископаемые. Это своего рода элементы, из которых составлены все ископаемые. Таких компонентов оказывается всего семь: графит, графитовая окись, карбоид, гумусовое вещество, битумное вещество, керогец, антракоид. [23]
В результате окисления в мягких условиях карбоиды, по крайней мере не слишком богатые углеродом, превращаются в гумусовые вещества. В более жестких условиях они дают графитовую окись, причем ее выход тем больше, чем карбоид богаче углеродом или чем выше был а температура его прокаливания. Эти реакции карбоидов устанавливают их отношение к гумусовым веществам и графитовой окиси. [24]
Замена таких малых и легкоподвижных частиц, как электроны, тяжелыми ионами кислорода и вызывает изменение свойств вещества. Каждый атомный слой решетки графита при этом превращается в гигантский катион, который создает вокруг себя сильное электрическое поле, способное захватывать и удерживать полярные молекулы. Таким образом, вся структура из типично металлической становится гетерополярной и гидрофильной. Это обусловливает резко выраженную способность графитовой окиси набухать, причем расстояния между атомными слоями увеличиваются. При благоприятных условиях в водной среде набухание может переходить в пептизацию. [25]
В первую очередь разрываются только слабые связи между атомными слоями, сами же слои остаются нетронутыми. Таковы реакции графита с сильными окислителями при невысоких температурах, которые приводят к образованию графитовой окиси. При этом кристаллы графита набухают, теряют электропроводность и становятся прозрачными. Рентгенографическое исследование их Доказывает, что структура атомных слоев графита при этом полностью сохраняется в графитовой окиси, но расстояния между ними сильно увеличиваются. Это обусловлено тем, что кислород входит между атомными слоями и захватывает подвижные электроны, находящиеся здесь. Вследствие этого графит теряет свои металлические свойства и превращается в диэлектрик - окись графита. [26]
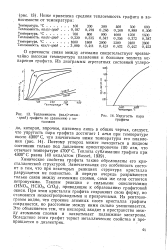 |
Упругость пара графита. [27] |
Химические свойства графита также обусловлены его кристаллической структурой. Замечательная его особенность состоит в том, что при некоторых реакциях структура кристалла разрушается не полностью. В первую очередь разрываются только связи между атомными слоями, сами же слои остаются нетронутыми. Таковы реакции с сильными окислителями ( HNO3, НС1О3, СгО3), приводящие к образованию графитовой окиси. При этом кристаллы графита сохраняют свою форму, но становятся неэлектропроводными и прозрачными. Из рентгенограмм видно, что строение атомных слоев кристалла графита сохраняется, но расстояние между ними сильно увеличивается. Это объясняется тем, что кислород входит в пространство между атомными слоями и захватывает подвижные электроны. Вследствие этого графит теряет металлические свойства и превращается в диэлектрик. [28]
При окислении алмаза и алифатических соединений при низких температурах этого никогда не происходит. Это следует понимать так, что и в этом случае не происходит полного разрушения молекулярной структуры графита, которая несомненно родственна и генетически связана с ароматической структурой органических соединений. Однако из этого не следует делать вывод, что графит имеет ароматическую структуру, а алмаз - алифатическую. Такое мнение основано лишь на внешнем сходстве и совершенно не соответствует действительности. В результате окисления графита металлическая связь между его атомными слоями разрушается, и он превращается в графитовую окись, которая имеет ароматическую структуру, так же как и бензол-карбоновые кислоты. [29]
Страницы: 1 2