Биогенез
Cтраница 1
Биогенез мРНК у эукариот существенно отличается не только механизмом регуляции транскрипции, но и многоступенчатостью формирования активной молекулы. До открытия феномена сплайсинга ( от англ, splicing - созревание, сращивание) мРНК было известно, что многие мРНК эукариот синтезируются в виде гигантских высокомолекулярных предшественников ( пре-м РНК), которые уже в ядре подвергаются посттранскрипционному процессингу. Предполагали, что процессинг включает удаление длинных 5 - и З - концевых участков, которые якобы выполняют регуляторные функции. Как оказалось, ген эукариот является не непрерывной, а мозаичной структурой, содержащей наряду с кодирующими ( экзоны) также некодирующие ( интроны) последовательности. Фермент РНК-полимераза катализирует транскрипцию как экзонов ( от англ, exit - выход, поскольку продукты транскрипции-участки мРНК - выходят из ядра в цитоплазму и выполняют функцию матрицы в синтезе белка), так и нитронов с образованием гетерогенной ядерной РНК ( гяРНК), называемой также первичным транскриптом. Термин интроны означает вставочные, нетранслирующие последовательности нуклеотидов в ДНК эукариот. Этот термин применим и к вставочным нуклеотидным последовательностям первичного РНК-транскрипта. [1]
Биогенез холестерина широко изучен и результаты суммированы ниже. Сквален тоже образуется из меченой уксусной кислоты; он оказался предшественником холестерина, что было обнаружено но биогенному превращению С14 - меченого сквалена в холестерин. В этом превращении метильные группы а, Ъ и d сквалена, очевидно, теряются, а метиль-ная группа с, возможно, мигрирует к С-13 холестерина, образуя ангулярную метильную группу стероида. Ланостерин ( найденный в жире шерсти овец) тоже образуется из сквалена. И в этом случае требуется миграция одной ме-тильной группы ( группа с) в сквалене в ангулярное положение при С-13 ланостерола, чтобы обеспечить общность скелета обоих веществ. [2]
Биогенез холестерина широко изучен и результаты суммированы ниже. Сквален тоже образуется из меченой уксусной кислоты; он оказался предшественником холестерина, что было обнаружено по биогенному превращению С14 - меченого сквалена в холестерин. В этом превращении метильные группы я, b и d сквалена, очевидно, теряются, а метиль-ная группа с, возможно, мигрирует к С-13 холестерина, образуя ангулярную метильную группу стероида. Ланостерин ( найденный в жире шерсти овец) тоже образуется из сквалена. И в этом случае требуется миграция одной ме-тильной группы ( группа с) в сквалене в ангулярное положение при С-13 ланостерола, чтобы обеспечить общность скелета обоих веществ. [3]
Биогенез лигнина [39] можно разделить на три стадии: образование низкомолекулярных предшественников, например шикимовой кислоты и соединений фенилпропанового ряда, превращение в спирты ( см. формулы I-III) и их гликозиды и дегидрогенизацию этих спиртов с образованием высокомолекулярного лигнина. Здесь они контактируют с ферментом р-глюкозидазой, которая освобождает гликозиды с образованием спиртов I-III, участвующих в дальнейшем синтезе лигнина при помощи фенолдегидрогеназ, представленных лакказой и пероксидазой. Ферменты образуют радикалы путем отделения водорода от фенольной группы, далее образующие олиго-меры и полимеры лигнина. [4]
Биогенез других природных пиридонов может иметь смешанный характер. Например, атомы С1, С5 и С6, а также бензольное кольцо антибиотика тенеллина 6.149 происходят из аминокислоты тирозина, а С2, СЗ, С4 вместе с боковой цепью представляют собой остаток пентакетидного предшественника. Продуцентом вещества 6.149 является микроскопический гриб Beauveria tenella ( боверия тонкая), интересный тем, что вызывает тяжелые грибковые заболевания насекомых, вредящих сельскому хозяйству. Это свойство грибов боверия использовано с целью приготовления препарата для биологической борьбы с колорадским жуком и другими вредителями. [5]
Схема биогенеза морфина, предложенная Робинсоном, предусматривает сопровождающееся окислением соединение двух ароматических колец норлауданозолина. Меченный С14 норлауданозо-лин оказался эффективным предшественником морфина, кодеина, тебаина и папаверина. [6]
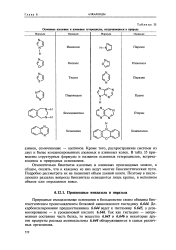 |
Основные азоловые и азиновые гетероциклы, встречающиеся в природе. [7] |
Относительно биогенеза азоловых и азиновых производных можно, в общем, сказать, что к каждому из них ведут многие биосинтетические пути. Подробно рассмотреть их не позволяет объем данной книги. Поэтому в последующих разделах вопросы биосинтеза освещаются лишь кратко, в неполном объеме или опускаются вовсе. [8]
Проблема биогенеза полиацетиленовых соединений представляет собой весьма сложную научную задачу, изучению различных аспектов которой посвящено большое число работ. Современные представления оо основных путях их биосинтеза в растениях основываются как на экспериментальных данных, полученных с помощью меченых атомов, так и на структурных корреляциях между отдельными типами этих соединений. Как и во всех исследованиях подобного рода, необходимо было прежде всего решить вопрос о биогенетическом принципе построения углеродной цепи полиацетиленовых соединений, выяснить пути образования тройной связи, установить биогенетическое родства между отдельными полиацетиленовыми структурами и разобраться в общих биохимических закономерностях их взаимных превращений. Несмотря на то, что все эти работы начались сравнительно недавно, полученные результаты уже сейчас позволяют ответить на многие иа поставленных вопросов и дают возможность достаточно определенно представить общую картину биогенеза полиацетиленовых соединений. [9]
Механизм биогенеза изохинолиновых алкалоидов еще не выяснен, но нет недостатка в предположениях в этом направлении. [10]
Понимание биогенеза природных соединений не только способствует расшифровке их строения, но открывает новые пути, возможности и принципы органического синтеза. [11]
Изучение биогенеза природных полиинов в настоящее время ведется очень интенсивно. [12]
В биогенезе гомоапорфинов, например флорамультина ( 241), фенетилизохинолиновый скелет претерпевает менее глубокие трансформации, чем в процессе биосинтеза колхицина. [13]
В начале биогенеза сквалена ( разд. [14]
Третий тип биогенеза состоит в окислительном расщеплении и последующей рециклизации циклических предшественников. [15]
Страницы: 1 2 3 4