Окраска - раствор - комплекс
Cтраница 2
В пробирку наливают - 0 5 мл 0 2 М раствора Bi ( NOs) 3, добавляют к нему по каплям 0 1 М раствор КЛ до выделения осадка ВПз. Отмечают окраску раствора комплекса. [16]
Для измерения интенсивности окраски раствора титанового комплекса с перекисью водорода в кислой среде применимы все методы колориметрических определений. Однако следует иметь в виду, что при длительном хранении растворов стандартной серии перекись водорода разлагается и это приводит к обесцвечиванию растворов. Поэтому в растворы стандартной серии время от времени добавляют перекись водорода. [17]
Для измерения интенсивности окраски раствора комплекса ванадия с перекисью водорода в кислой среде применимы все методы. [18]
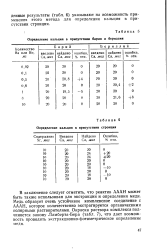 |
Определение кальция в присутствии стронция. [19] |
В заключение следует отметить, что реактив АААН может быть также использован для экстракции и определения меди. Медь образует очень устойчивое комплексное соединение с АААН, которое количественно экстрагируется органическими полярными растворителями. Окраска раствора комплекса подчиняется закону Ламберта-Бера ( табл. 7), что дает возможность проводить экстракционно-фотометрическое определение меди. [20]
Соли лития взаимодействуют с этим реагентом в водно-органической среде ( ацетон, диоксан, диметилформамид, этанол) в присутствии щелочи. Окраска растворов комплексов лития с реагентами устойчива в течение 2 час. [21]
К 1 2 мл водного раствора соли лития прибавляют 0 2 мл 0 002 М раствора реагента в диметилформамиде, 0 2 мл 0 2 Л раствора КОН и 4 4 мл ацетона и перемешивают. В выбранных условиях окраска реагента и продукта взаимодействия его с литием устойчива в течение 1 5 час. Изменение окраски раствора комплекса указывает на присутствие лития. [22]
В пробирку наливают - 0 5 мл 0 2 М раствора Bi ( NO3) a, добавляют к нему по каплям 0 1 М раствор K. I до выДеления осадка ВПз - Отмечают цвет осадка. Отмечают окраску раствора комплекса. [23]
Комплексы оснований с ацидо-кисдотамя металлов применяют для определения Си в виде пиридин-родапидпого комплекса, Ti в виде диаптипирилметан-родапидного комплекса и др. Обе последние группы обычно применяют в К. Мм в виде псрманга-ната, и др. 8) Для определения анионов применяют часто реакции обесцвечивания ими окрашенных комплексов металлов; так, для определения фторид-ионов измеряют ослабление окраски растворов перокисного комплекса титана вследствие связывания титана во фторидный комплекс. Применяют также реакции синтеза; напр. Кроме обычных типов реакций компдексо-образования, окисления-восстановления и синтеза, используются также каталнтич. [24]
Сопоставление приведенных выше данных показывает, что в растворах фторного железа наблюдается автокомплексообразо-вание при незначительной степени электролитической диссоциации. Правильность последнего заключения [66,71] подтверждается многочисленными качественными наблюдениями. Растворы FeF3 не окрашиваются от прибавления роданида, сульфосалициловой или салициловой кислоты, антипирина. На ослаблении окрасок растворов комплексов солей Fe с этими реагентами основаны многочисленные методы колориметрического определения фтора. Было также исследовано [76 ] влияние введения ионов F на изменение спектра поглощения упомянутых выше окрашенных комплексов железа. [25]
Страницы: 1 2