Окраска - вещество
Cтраница 1
 |
Кривая титрования 0 1 н. раствора СНзСООН 0 1 н. раствором МЬЬОН. [1] |
Окраска веществ зависит от наличия в их молекуле особых атомных группировок - хромофоров. Хромофор в органических соединениях чаще всего представляет собой систему сопряженных ( чередующихся) простых и двойных связей. Чем больше длина цепи сопряжения, тем более сильно окрашено вещество. [2]
Окраска вещества может служить одной из его энергетических характеристик. [3]
Окраска вещества обусловлена поглощением молекулами этого вещества квантов света в видимой области спектра. [4]
Окраска вещества, содержащего хромофорные группы, усиливается при введении в молекулу органического соединения особых групп атомов, которые получили название ауксохромов. [5]
Окраска вещества обусловлена электронными переходами между нижним и верхним d - уровня-ми, так как величина QDq соответствует обычно длине волны видимой части электромагнитного спектра. Теория объясняет также магнитные свойства этих соединений. В зависимости от расположения в решетке ионы кобальта двух - или трехвалентны, и формула соединения имеет вид Со Со Ю Если бы d - уровни были полностью вырожденными, как в свободном ионе, на одну молекулу соединения приходилось бы одиннадцать неспаренных электронов, так как, согласно правилу Гунда, в Со31 ( электронная конфигурация d6) и в Со2 1 ( конфигурация d -) расположение спинов имеет соответственно такой вид: f f f f f и f - J - f j f f t При сильном расщеплении d - уровня ситуация меняется. Окружение иона Со3 расщепляет d - уровень на три нижних и два верхних. При большом расщеплении правило Гунда неприменимо, и шесть d - электронов заполняют только три нижних уровня и имеют спаренные спины; поэтому Со3 - ион не имеет магнитного момента. Окружение Со2 1 расщепляет d - уровни иона на два нижних и три верхних уровня. Четыре из семи d - электронов заполняют попарно два нижних уровня, оставшиеся три электрона заполняют три верхних уровня ( по одному на каждом уровне), так что их спины параллельны. Таким образом, именно благодаря наличию трех неспаренных электронов Со3О4, как показывает эксперимент, обладает результирующей намагниченностью. [6]
Окраска вещества зависит от избирательного поглощения части лучей видимого спектра. Цвет вещества в проходящем свете всегда является дополнительным к цвету лучей, поглощаемых этим веществом. [7]
Окраска вещества зависит от избирательного поглощения части лучей видимого спектра. Цвет вещества в проходящем свете всегда является дополнительным к цвету лучей - поглощаемых этим веществом. [8]
Окраска вещества зависит от избирательного поглощения части лучей видимого спектра. Цвет вещества в проходящем свете всегда является дополнительным к тому, который веществом поглощается. В табл. 7 даны длины волн частей видимого спектра, соответствующие спектральные цвета и цвета, дополнительные к ним. [9]
Интенсивность окраски веществ, охватываемых этим правилом, значительно выше, чем интенсивность окраски сходного строения соединений, окраска которых вызывается просто хромофорным действием элементов. По этой причине цветные аналитические реакции, у которых окраска образующихся продуктов реакции связана с правилом Гофмана - Резеншека, обладают высокой чувствительностью при хорошей избирательности действия. [10]
По окраске вещества можно до некоторой степени судить о его природе, так как большинство органических соединений при обычном освещении не окрашено. [11]
Чем объясняется окраска веществ. [12]
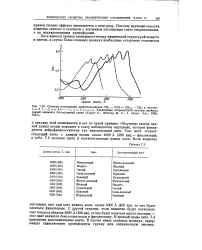 |
Спектры поглощения диметщшолиенов СН3 - ( СН СН П - СН3 в гексане. [13] |
Поэтому изучение окраски вещества связано в основном с изучением поглощения света сопряженными, а не изолированными хромофорами. [14]
Повышение интенсивности окраски вещества происходит при наличии в молекулах ионов, которые резко усиливают поглощение квантов света. [15]
Страницы: 1 2 3 4