Оксалат
Cтраница 4
 |
Зависимость растворимости оксалатов Th, Ce, La и Sm от концентрации H2SO4.| Зависимость - lg Пр оксалатов. [46] |
Оксалаты РЗЭ используются для группового их отделения от тория. [47]
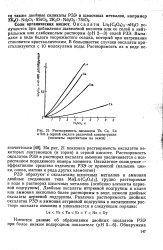 |
Растворимость оксалатов Th, Ce, La. [48] |
Оксалаты Lnj ( СаО з пН2О получаются при добавлении щавелевой кислоты или ее солей к нейтральным или слабокислым растворам ( рН 2 - 3) солей РЗЭ. Выпадают в виде белого творожистого осадка, который при нагревании становится кристаллическим. В большинстве случаев оксалаты кристаллизуются с 10 молекулами воды. [49]
Оксалат Ри ( III) - Р СгО з - ЭНаО получается при добавлении к кислому ( 1 - 1 5 N) раствору Ри ( III) кристаллической щавелевой кислоты или оксалата аммония ( натрия) в количестве, достаточном для полного осаждения плутония и для насыщения раствора. [50]
Оксалат Am ( III) трудно растворим в разбавленных кислотах. [51]
Оксалат бария и кальция нерастворимы в воде. [52]
Оксалаты бария и кальция нерастворимы в воде. [53]
Оксалат лития может служить реагентом для определения Са, Sr, Ba, Ag, Pb, Cu и других. Наибольшее практическое значение имеет определение Са 1 1, так как его определение другими реагентами затруднено вследствие довольно высокой растворимости осадков. [54]
Страницы: 1 2 3 4