Оксалат - железо
Cтраница 2
Было показано [31], что оксалат железа окисляет перекись водорода в фиолетовом и ультрафиолетовом свете; эта реакция легко сенсибилизируется хлорофиллом. Но общее количество кислорода, получившееся в экспериментах Хилла, требовало бы наличия перекиси в хлоропластах в концентрации 0 1 моля на 1 л, что неправдоподобно. Далее, на 1 грамм-атом восстановленного иона железа приходится только половина грамм-атома кислорода. [16]
Для этого необходимо было заменить оксалат железа ( II) на цитрат железа ( II), так как при значительном увеличении окислительно-восстановительного потенциала раствора оксалата железа в нем выпадает осадок. [17]
Написать уравнения реакций: разложения оксалата железа; горения железа, учитывая, что продуктом горения является закись-окись железа. [18]
Нани сать уравнение реакции разложения оксалата железа, учитывая; что в реакции принимает участие кислород воздуха. [19]
Удовлетворительную защиту дает также обработка в оксалате железа, при которой образуется желтая пленка декоративного вида. [20]
Примером может служить определение золы в оксалате железа. [21]
Установлено, что при рН 4 растворимость оксалата железа повышается настолько, что ( учитывая малые концентрации железа, в которых оно может находиться, в частности, в природных водах) можно не опасаться адсорбции его оксалатом кальция в заметной степени. Правда, при рН RSS 4 растворимость оксалата кальция повышается ( возрастает примерно в 1 5 раза), но это повышение растворимости может быть устранено введением достаточного избытка оксалат-ионов. [22]
Наполнить пробирку на V4 ее объема порошком оксалата железа FeC2O4 и укрепить в штативе горизонтально. [23]
Наполнить пробирку на / 4 ее объема порошком оксалата железа FeCr2O4 и укрепить в штативе горизонтально. [24]
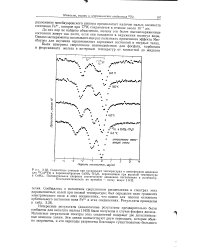 |
Скоростные спектры при нескольких температурах и атмосферном давлении. [25] |
Интересные результаты ( аналогичные результаты предварительно были сообщены для оксалата железа [143]) были получены в случае фосфата железа. [26]
Оксалатирсвание - нанесение на поверхность заготовки слоя солей щавелевой кислоты НООС-СООН ( оксалата железа), образующегося при растворении железа в рабочем растворе, в котором должны содержаться активаторы - соли NaCl, КС1, NaB2 и окислители - двухромокислый калий К2Сг2О7, пер-манганат калия КМпО4 и другие. Процесс используется для обработки высоколегированных сталей, цветных металлов и сплавов. Прочное покрытие, хорошо адсорбирующее смазку, образуется при выдержке в течение 15 мин. В мыльном растворе на оксалатном покрытии образуется пленка металлических мыл, прочно сцепленная с поверхностью заготовки. [27]
Окись железа ( П) образуется в виде черного пирофорного порошка при нагревании оксалата железа ( П) в вакууме. Даже непродолжительное нагревание окиси железа до высокой температуры делает его менее реакционноспособным. [28]
Окись железа () FeO ( вюстит) получают в виде черного порошка путем термического разложения оксалата железа ( П) в отсутствие воздуха. После сильного прокаливания высокая реакционная способность FeO несколько снижается. Гидроокись железа ( П) Fe ( OH) 2 в отсутствие воздуха осаждается щелочами из растворов солей Fe ( II) в виде белого хлопьевидного осадка. [29]
Так, для железа прочность комплексов с ЭДТА на 10 - 15 порядков больше, чем у оксалатов железа. [30]
Страницы: 1 2 3 4