Оксалат - железо
Cтраница 3
Термическое разложение оксалатов Со и Ni в атмосфере азота идет по схеме ЭС204 2С02 Э, тогда как оксалат железа разлагается до окисла. [31]
Для получения пентакарбоаила железа Fe ( CO) 5 с хорошим выходом применяется тонкодисперсное железо, полученное восстановлением оксалата железа водородом или дистилляцией железной амальгамы в вакууме. [32]
Термическое разложение оксалатов Со и Ni в атмосфере азота идет по схеме ЭСаО - 2СОа Э, тогда как оксалат железа разлагается до окисла. [33]
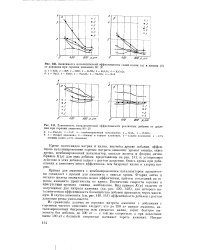 |
Зависимость каталитической эффективности солей калия ( а и натрия ( б.| Зависимость каталитической эффективности различных добавок от давления при горении аммонита 80. 20. [34] |
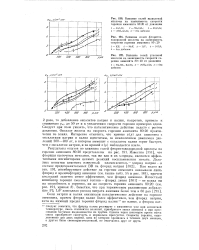
Кроме галогенидов натрия и калия, изучены другие добавки, эффективно катализировавшие горение нитрата аммония: хромат свинца, окись хрома, комбинированный катализатор, оксалат железа и фторид лития. Кривые К ( р) для этих добавок представлены на рис. 141, а; ускоряющее действие и этих добавок падает с ростом давления. Окись хрома при добавлении к аммониту менее эффективна, чем бихромат калия и хлорид натрия. [35]
Для этого необходимо было заменить оксалат железа ( II) на цитрат железа ( II), так как при значительном увеличении окислительно-восстановительного потенциала раствора оксалата железа в нем выпадает осадок. [36]
Пигмент зеленый В получается в очень мелких частицах, пригодных для наполнения резины, если на суспензию бисульфитного соединения ( VI) в водном ализариновом масле подействовать раствором оксалата железа и щавелевой кислоты с последующим осаждением продукта раствором соды. [37]
Нейтральный оксалат калия С2О4К2 - Н2О легко растворим в воде; кислый оксалат калия С2О4НК плохо растворим в воде; тетраоксалат калия имеет состав С2О4НК - С2Н2О4 - 2Н2О; оксалат кальция С2О4Са - Н2О, маленькие моноклинные таблички, очень плохо растворим в воде и уксусной кислоте, легко-в соляной и серной кислотах; оксалат серебра C2O4Ag2, незначительно растворим в воде; оксалат железа C204Fe - 2H2O, желтый порошок, незначительно растворим в воде; феррооксалат калия К2Ре ( С204) 2 - Н2О, сильный восстановитель. [38]
Следует при этом указать, что каталитическое действие падало с ростом давления. Оксалат железа на скорость горения аммонита 80: 20 практически не влиял. Интересно отметить, что кривые и ( р) для аммонита с оксалатами натрия и калия идентичны, за исключением диапазона давлений 200 - 400 ат, в котором аммонит с оксалатом калия горит быстрее, чем с оксалатом натрия, и на кривой и ( р) наблюдается плато. [40]
Кривая для аммонита с комбинированным катализатором практически совпадает с кривой для аммонита с окисью хрома. Фторид лития и оксалат железа значительно менее эффективны, причем последний на горение аммонита практически не влиял. Увеличение скорости горения в присутствии хромата свинца наибольшее. Вид кривых К ( р) отличен от полученных для нитрата аммония ( см. рис. 120 - 123), для которого каталитическая эффективность большинства добавок проходила через максимум. В случае аммонита ( см. рис. 140, 141) эффективность добавок с ростом давления резко уменьшается. [41]
Рек [419] нашел, что ток обмена в растворе оксалата железа является линейной функцией заполнения поверхности только в присутствии н-гексилового спирта; для таких веществ, как тимол, полиоксиэтиленовые эфиры лауриловой кислоты и додецилсульфат натрия, зависимость тока обмена от 0 отклоняется от линейной. [42]
Штатив железный с лапкой. Сухие реактивы: соль Мора; железо ( стружки); оксалат железа ( II); бертолетова соль; едкое кали. [43]
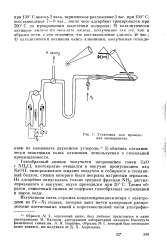 |
Установка для проведения эксперимента. [44] |
С до прекращения выделения водорода; 8) каталитически активное железо из оксалата железа. [45]
Страницы: 1 2 3 4