Оксалат - лантан
Cтраница 1
Оксалат лантана несколько растворим в минеральных кислотах, оксалат же церия растворяется в них значительно слабее, и в дальнейшем, при переходе к следующим элементам группы РЗЭ, растворимость понижается до десятых долей миллиграмма на 1000 г раствора. В соляной кислоте растворимость оксалатов плавно понижается от лантана к неодиму и европию, составляя около 1 г на 1000 г раствора для этих элементов, и вновь повышается при переходе к гадолинию. [1]
Оксалат лантана малорастворим в воде [4] и может быть осажден из водных растворов солей лантана щавелевой кислотой. [2]
Насыщенный раствор оксалата лантана, применяемый в опытах, приготовлялся из соли, синтезированной в присутствии радиоактивного изотопа ( Lauo) и заражался исследуемым микрокомпонентом. [3]
Распределение Pu ( IV) между оксалатом лантана и раствором может происходить и по закону Хлопина и по логарифмическому закону в зависимости от условий проведения соосаж-дения. [4]
Следовательно, 98 % MsThn было отделено от тория и осаждено с оксалатом лантана. [5]
Подкислением раствора 30 % - ной азотной кислотой до рН 6 6 выделяют оксалат лантана, практически не содержащий Рг, и только лишь следы Nd. Для получения чистейшего лантана из исходного препарата, содержащего 10 % окислов Рг и Nd, необходимо 3 - 4 фракционирования. [6]
При подкислении раствора 30 % - ной азотной кислотой до рН 6 6 выделялся оксалат лантана, практически не содержащий празеодим, в котором обнаруживали только следы неодима. [7]
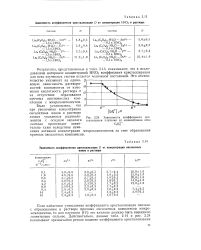 |
Зависимость коэффициентов кристаллизации D от концентрации HNO3 в растворе.| Зависимость коэффициента кристаллизации плутония от концентрации иона 2. [8] |
Было установлено, что при увеличении концентрации оксалатных ионов в растворе захват указанных радиоэлементов с осадком оксалата лантана происходит значительно хуже вследствие изменения активной концентрации микрокомпонентов за счет образования прочных оксалатных комплексов. [9]
Соединение LaFg HgO получают обработкой концентрированных растворов хлорида лантана фтористоводородной кислотой или фторидом калия, а также кипячением оксалата лантана с раствором фторида щелочного металла. [10]
В соответствии с приведенными в начале статьи соображениями величины коэффициентов распределения примеси Fe3 при кристаллизации двойной соли лантана аммония сернокислого и оксалата лантана очень близки к нулю. Однако и при весьма незначительном уровне величин коэффициентов распределения этой примеси Fe3 ( порядка 0 0001 и меньше) на степени очистки кристаллов заметно сказывается захват микрокомпонента твердой фазой. [11]
Значительные количества оксалатов иттрия, и особенно скандия, растворяются в горячих концентрированных растворах щавелевокислых солей натрия, калия и аммония. Оксалат лантана в растворах других оксалатов почти не растворяется. На различной растворимости оксалатов Sc, Y, La и элементов семейства лан-танидов в горячем концентрированном растворе ( МН4ЬС2О4 основан один из методов их разделения. [12]
Значительные количества оксалатов иттрия, и особенно скандия, растворяются в горячих концентрированных растворах щавелевокислых солей натрия, калия и аммония. Оксалат лантана в растворах других оксалатов почти не растворяется. На различной растворимости оксалатов Sc, Y, La и элементов семейства лан-танидов в горячем концентрированном растворе ( NH4) 2C2O4 основан один из методов их разделения. [13]
Это различие обусловлено отчасти неполной диссоциацией, а отчасти образованием комплексных ионов. Иными словами, при диссоциации оксалата лантана образуются не только простые ионы La444 и С2О4, как предполагается при определении растворимости по данным электропроводности; наряду с этим в насыщенном растворе имеются в заметном количестве комплексные ионы, содержащие как лантан, так и оксалат. Поэтому при использовании результатов, получаемых посредством измерений электропроводности насыщенных растворов мало растворимых электролитов, следует соблюдать осторожность - Определение основности кислот. [14]
Метод основан на извлечении Np совместно с U и Ри после их окисления персульфатом аммония в присутствии AgNO3 и последующем восстановлении Np ( VI) до Np ( IV), который остается в маточном растворе. Окончательное выделение Np проводят соосаждением с гидроксидом и оксалатом лантана. [15]
Страницы: 1 2