Оксалат - натрий
Cтраница 2
 |
Кристаллы оксалата кальция ( под микроскопом. [16] |
Оксалат натрия, как вещество, осаждающее ионы кальция, применяется в медицине в качестве антикоагулянта, предотвращающего свертывание крови при добавлении всего 1 - 2 мг его на 1 мл крови. [17]
Оксалат натрия не гигроскопичен, кристаллизуется без кристаллизационной воды, может быть легко проверен на чистоту по прописям, данным Збгепзеп ом, 1 и по стр. [18]
Оксалат натрия применяется в качестве исходного вещества для установки титра перманганата. [19]
Оксалат натрия применяют в качестве исходного вещества для установки титра перманганата. [20]
Оксалат натрия для этой цели не применяют вследствие сильного отклонения конечной точки титрования от эквивалентной. Титрование проводят лишь в водном растворе, так как в растворах, содержащих спирт или ацетон, эквивалентная точка неотчетлива. При титровании 0 1 М раствором оксалата калия или аммония скачок потенциала в эквивалентной точке при 25 составляет 25 мв, а при 60 - 70 - 70 мв. [21]
Оксалат натрия N820204 очищают перекристаллизацией из водного раствора и высушивают при 20О - 220 С. Перед взятием точной навески соль следует подсушить в течение 1 ч при 11О - 120 С. [22]
Оксалат натрия кристаллизуется без воды. [23]
Оксалат натрия не подвергается заметному разложению при нагревании даже до 240, но в этом случае следует применять электрический сушильный шкаф, потому что в шкафу, обогреваемом газом, может происходить поглощение сернистых соединений из продуктов сгорания газа. Обычно в нагревании до таких высоких температур нет необходимости, если нет подозрения, что оксалат содержит бикарбонат натрия или окклюдированную воду. [24]
Оксалат натрия непосредственно не титруется кислотой, так как его водный раствор не обладает сильно щелочной реакцией подобно карбонату или тетраборату натрия. Его предварительно переводят в карбонат натрия путем нагревания в платиновом тигле. Образующийся при этом карбонит натрия термически не разлагается даже при температуре плавления и может быть использован для установки титра кислоты. [25]
Оксалат натрия или щавелевую кислоту всыпают в пробирку для взвешивания и берут навески в 4 - 5 заранее подготовленные колбы на 200 мл ( стр. [26]
Оксалат натрия Na2C2O4 выделяется из водного раствора в виде безводных негигроскопичных кристаллов. Обычно его используют вместо щавелевой кислоты для установления титра раствора перманганата, поскольку он получается в чистом виде легче, чем свободная кислота. Кроме того, оксалат натрия используют для установления титра растворов кислот, применяемых в ацидиметрии. Первоначальное количество оксалата натрия переводят количественно путем прокаливания в карбонат натрия, который получается при этом в очень чистом состоянии. Его применяют в качестве основания для титрования раствора кислоты. [27]
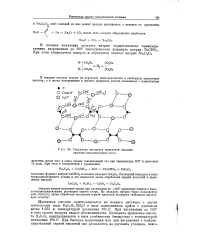 |
Структура дпгидрата щавелевой кислоты, ( проекция перпендикулярна оси Ь. [28] |
Оксалат натрия получают также при нагревании до - 285 древесных опилок с высококонцентрированным раствором едкого натра. Из оксалата натрия через кальциевую соль ( СаС204) путем обработки последней серной кислотой получают свободную щавелевую кислоту. [29]
Оксалат натрия очищают, перекристаллизовывая из воды, и высушивают при 240 - 250 С. На аналитических весах точно отвешивают в бюксе 0 3350 г Na2C2O4 или 0 3152 г Н2С2О4 - 2Н2О, переносят в мерную колбу на 250 мл, растворяя в холодной дистиллированной воде. Раствор доводят до метки дистиллированной водой и перемешивают. [30]
Страницы: 1 2 3 4